
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
 јхЙЩNO2ЎўSO2ЎўCOөИУРәҰЖшМе¶ФҙуЖш»·ҫіөДОЈәҰЈ¬КЗИЛАаөД№ІН¬Ч·ЗуЈ®
јхЙЩNO2ЎўSO2ЎўCOөИУРәҰЖшМе¶ФҙуЖш»·ҫіөДОЈәҰЈ¬КЗИЛАаөД№ІН¬Ч·ЗуЈ®
| ||
| јУС№ |
| ||
| јУС№ |
| 3 |
| 2 |
| 3 |
| 2 |
| 8 |
| 3 |
| 8 |
| 3 |

ЈЁ7·ЦЈ©СРҫҝNO2ЎўSO2 ЎўCOөИҙуЖшОЫИҫЖшМеөДҙҰАнҫЯУРЦШТӘТвТеЎЈ
ЈЁ1Ј©NO2ҝЙУГЛ®ОьКХЈ¬ПаУҰөД»ҜС§·ҙУҰ·ҪіМКҪОӘ ЎЈАыУГ·ҙУҰ6NO2Ј« 8NH3 7N2Ј«12 H2OТІҝЙҙҰАнNO2ЎЈөұЧӘТЖ1.2molөзЧУКұЈ¬ПыәДөДNO2ФЪұкЧјЧҙҝцПВКЗ LЎЈ
7N2Ј«12 H2OТІҝЙҙҰАнNO2ЎЈөұЧӘТЖ1.2molөзЧУКұЈ¬ПыәДөДNO2ФЪұкЧјЧҙҝцПВКЗ LЎЈ
ЈЁ2Ј©ТСЦӘЈә2SO2ЈЁgЈ©+O2ЈЁgЈ© 2SO3ЈЁgЈ© ҰӨH="-196.6" kJЎӨmol-1
2SO3ЈЁgЈ© ҰӨH="-196.6" kJЎӨmol-1
2NOЈЁgЈ©+O2ЈЁgЈ© 2NO2ЈЁgЈ© ҰӨH="-113.0" kJЎӨmol-1
2NO2ЈЁgЈ© ҰӨH="-113.0" kJЎӨmol-1
ўЩ РҙіцNO2Сх»ҜSO2өДИИ»ҜС§·ҪіМКҪ
ўЪТ»¶ЁМхјюПВЈ¬Ҫ«NO2УлSO2ТФМе»эұИ1:2ЦГУЪГЬұХИЭЖчЦР·ўЙъЙПКц·ҙУҰЈ¬ПВБРДЬЛөГч·ҙУҰҙпөҪЖҪәвЧҙМ¬өДКЗ ЎЈ
aЈ®МеПөС№ЗҝұЈіЦІ»ұд bЈ®»мәПЖшМеСХЙ«ұЈіЦІ»ұд
cЈ®SO3әНNOөДМе»эұИұЈіЦІ»ұд dЈ®ГҝПыәД1 mol SO3өДН¬КұЙъіЙ1 molNO2
ўЫІвөГЙПКц·ҙУҰЖҪәвКұNO2УлSO2Ме»эұИОӘ1:6Ј¬ФтЖҪәвіЈКэKЈҪ ЎЈ
ЈЁ3Ј©COҝЙУГУЪәПіЙјЧҙјЈ¬·ҙУҰ·ҪіМКҪОӘ
COЈЁgЈ©+2H2ЈЁgЈ© CH3OHЈЁgЈ©ЎЈCOФЪІ»Н¬ОВ¶ИПВөДЖҪәвЧӘ»ҜВКУлС№ЗҝөД№ШПөИзПВНјЛщКҫЎЈ
CH3OHЈЁgЈ©ЎЈCOФЪІ»Н¬ОВ¶ИПВөДЖҪәвЧӘ»ҜВКУлС№ЗҝөД№ШПөИзПВНјЛщКҫЎЈ
ёГ·ҙУҰҰӨH 0ЈЁМоЎ°>Ўұ»тЎ° <ЎұЈ©ЎЈКөјКЙъІъМхјюҝШЦЖФЪ250ЎжЎў1.3ЎБ104kPaЧуУТЈ¬СЎФс
ҙЛС№ЗҝөДАнУЙКЗ ЎЈ
ЈЁ10·ЦЈ©СРҫҝNO2ЎўSO2 ЎўCOөИҙуЖшОЫИҫЖшМеөДҙҰАнҫЯУРЦШТӘТвТеЎЈ
ЈЁ1Ј©ТСЦӘЈә2SO2ЈЁgЈ©+O2ЈЁgЈ©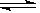 2SO3ЈЁgЈ© ҰӨHЈҪЈӯ196.6 kJЎӨmol-1
2SO3ЈЁgЈ© ҰӨHЈҪЈӯ196.6 kJЎӨmol-1
2NOЈЁgЈ©+O2ЈЁgЈ©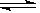 2NO2ЈЁgЈ© ҰӨHЈҪЈӯ113.0 kJЎӨmol-1
2NO2ЈЁgЈ© ҰӨHЈҪЈӯ113.0 kJЎӨmol-1
Фт·ҙУҰNO2ЈЁgЈ©+SO2ЈЁgЈ©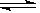 SO3ЈЁgЈ©+NOЈЁgЈ©өДҰӨHЈҪ kJЎӨmol-1ЎЈ
SO3ЈЁgЈ©+NOЈЁgЈ©өДҰӨHЈҪ kJЎӨmol-1ЎЈ
ЈЁ2Ј©Т»¶ЁМхјюПВЈ¬Ҫ«NO2УлSO2ТФМе»эұИ1ЎГ2ЦГУЪГЬұХИЭЖчЦР·ўЙъЙПКц·ҙУҰЈ¬ПВБРДЬЛөГч·ҙУҰҙпөҪЖҪәвЧҙМ¬өДКЗ ЎЈ
aЈ®МеПөС№ЗҝұЈіЦІ»ұд bЈ®»мәПЖшМеСХЙ«ұЈіЦІ»ұд
cЈ®SO3әНNOөДМе»эұИұЈіЦІ»ұд dЈ®ГҝПыәД1 mol SO3өДН¬КұЙъіЙ1 mol NO2
ІвөГЙПКц·ҙУҰЖҪәвКұNO2УлSO2Ме»эұИОӘ1ЎГ6Ј¬ФтЖҪәвіЈКэKЈҪ ЎЈЈЁұЈБф2О»РЎКэЈ©
ЈЁ3Ј©COҝЙУГУЪәПіЙјЧҙјЈ¬·ҙУҰ·ҪіМКҪОӘCOЈЁgЈ©+2H2ЈЁgЈ©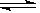 CH3OHЈЁgЈ©ЎЈ
CH3OHЈЁgЈ©ЎЈ
COФЪІ»Н¬ОВ¶ИПВөДЖҪәвЧӘ»ҜВКУлС№ЗҝөД№ШПөИзНјЛщКҫЎЈ
ёГ·ҙУҰҰӨH 0ЈЁМоЎ°>Ўұ»тЎ° <ЎұЈ©ЎЈКөјКЙъІъМхјюҝШЦЖФЪ250ЎжЎў1.3ЎБ104kPaЧуУТЈ¬СЎФсҙЛС№ЗҝөДАнУЙКЗ ЎЈ
ЈЁ12·ЦЈ©СРҫҝNO2ЎўSO2 ЎўCOөИҙуЖшОЫИҫЖшМеөДҙҰАнҫЯУРЦШТӘТвТеЎЈ
ЈЁ1Ј©NO2ҝЙУГЛ®ОьКХЈ¬ПаУҰөД»ҜС§·ҙУҰ·ҪіМКҪОӘ ЎЈ
ЈЁ2Ј©ТСЦӘЈә2SO2ЈЁgЈ©+O2ЈЁgЈ© 2SO3ЈЁgЈ© ҰӨH= ЎӘ196Ј®6 kJЎӨmol-1
2SO3ЈЁgЈ© ҰӨH= ЎӘ196Ј®6 kJЎӨmol-1
2NOЈЁgЈ©+O2ЈЁgЈ© 2NO2ЈЁgЈ© ҰӨH= ЎӘ113Ј®0 kJЎӨmol-1
2NO2ЈЁgЈ© ҰӨH= ЎӘ113Ј®0 kJЎӨmol-1
Фт·ҙУҰNO2ЈЁgЈ©+SO2ЈЁgЈ© SO3ЈЁgЈ©+NOЈЁgЈ©өДҰӨH= kJЎӨmol-1
SO3ЈЁgЈ©+NOЈЁgЈ©өДҰӨH= kJЎӨmol-1
Т»¶ЁМхјюПВЈ¬Ҫ«1 mol NO2Ул2 mol SO2ЦГУЪГЬұХИЭЖчЦР·ўЙъЙПКц·ҙУҰЈ¬ПВБРДЬЛөГч·ҙУҰҙпөҪЖҪәвЧҙМ¬өДКЗ ЎЈ
aЈ®МеПөС№ЗҝұЈіЦІ»ұд bЈ®»мәПЖшМеСХЙ«ұЈіЦІ»ұд
cЈ®SO3әНNOөДМе»эұИұЈіЦІ»ұд dЈ®ГҝПыәД1 mol SO3өДН¬КұЙъіЙ1 mol NO2
ІвөГЙПКц·ҙУҰЖҪәвКұNO2УлSO2ОпЦКөДБҝЦ®ұИОӘ1:6Ј¬ФтЖҪәвіЈКэKЈҪ ЎЈ
ЈЁ3Ј©COҝЙУГУЪәПіЙјЧҙјЈ¬·ҙУҰ·ҪіМКҪОӘCOЈЁgЈ©+2H2ЈЁgЈ© CH3OHЈЁgЈ©ЎЈCOФЪІ»Н¬ОВ¶ИПВөДЖҪәвЧӘ»ҜВКУлС№ЗҝөД№ШПөИзНјЛщКҫЎЈёГ·ҙУҰҰӨH 0ЈЁМоЎ°>Ўұ»тЎ° <ЎұЈ©ЎЈКөјКЙъІъМхјюҝШЦЖФЪ250ЎжЎў1Ј®3ЎБ104kPaЧуУТЈ¬СЎФсҙЛС№ЗҝөДАнУЙКЗ ЎЈ
CH3OHЈЁgЈ©ЎЈCOФЪІ»Н¬ОВ¶ИПВөДЖҪәвЧӘ»ҜВКУлС№ЗҝөД№ШПөИзНјЛщКҫЎЈёГ·ҙУҰҰӨH 0ЈЁМоЎ°>Ўұ»тЎ° <ЎұЈ©ЎЈКөјКЙъІъМхјюҝШЦЖФЪ250ЎжЎў1Ј®3ЎБ104kPaЧуУТЈ¬СЎФсҙЛС№ЗҝөДАнУЙКЗ ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com