CO和H
2与我们的生产和生活等方面密切相关.
(1)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.
已知:C(s)+O
2(g)=CO
2(g)△H=-393.5kJ.mol
-1H
2(g)+
O
2(g)=H
2O(g)△H=-242.0kJ.mol
-1CO(g)+
O
2(g)=CO
2(g)△H=-283.0kJ.mol
-1则C(s)与水蒸气反应制取CO和H
2的热化学方程式为
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ.mol-1
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ.mol-1
.标准状况下,V( CO):V(H
2)=1:l的水煤气22.4L,完全燃烧生成CO
2和水蒸气,放出的热量为
262.5kJ
262.5kJ
.
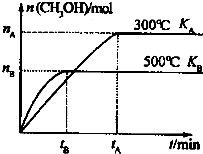
(2)一定条件下,在容积为3L的密闭容器中发生反应:CO(g)+2H
2(g)?CH
3OH(g),达平衡状态.根据图示回答:
①500℃时,从反应开始至达到平衡状态V(H
2)=
(用n
B、t
B表示)
②K
A 和K
B的关系是:K
A>
>
K
B,该反应的△H
<
<
0(填“>”、“=”或“<”).
③300℃达平衡时,将容器容积压缩到原来的
,其他条件不变,则v(正)
>
>
v(逆)(填“大于”、“等于”或“小于”).
(3)室内煤气泄漏造成人体中毒,是因为CO吸入肺中与输氧血红蛋白(HbO
2)发生反应:CO+HbO
2?O
2+HbCO,37℃时,K=220.当[HbCO]:[HbO
2]≥0.02时,即吸入CO与O
2物质的量浓度之比≥
1:11000
1:11000
时,人的智力会受损;把CO中毒的病人放入高压氧舱中解毒的原理是
氧气浓度增大,上述化学平衡逆向移动,使CO从血红蛋白中脱离出来
氧气浓度增大,上述化学平衡逆向移动,使CO从血红蛋白中脱离出来
.

 CO和H2与我们的生产和生活等方面密切相关.
CO和H2与我们的生产和生活等方面密切相关. O2(g)=H2O(g)△H=-242.0kJ.mol-1
O2(g)=H2O(g)△H=-242.0kJ.mol-1 O2(g)=CO2(g)△H=-283.0kJ.mol-1
O2(g)=CO2(g)△H=-283.0kJ.mol-1 ,其他条件不变,则v(正)______v(逆)(填“大于”、“等于”或“小于”).
,其他条件不变,则v(正)______v(逆)(填“大于”、“等于”或“小于”).
 Fe(s)+CO2(g) △H>O,其平衡常数可表示为
Fe(s)+CO2(g) △H>O,其平衡常数可表示为 ,已知1373K时K=0. 263。
,已知1373K时K=0. 263。  O2 (g)+Hb·CO(g),实验表明,Hb·CO的浓度即使只有Hb·O2浓度的2%,足以使人的智力受损,试回答: ①上述反应的平衡常数表达式为K=___。 ②已知37℃时,该反应平衡常数K=220,抽烟后,测得吸入肺部的空气中的CO和O2的浓度分别为1×10-6 mol/L和1×10-2mol/L,能否使人的智力受损____(填“能”或“否”),理由是___。
O2 (g)+Hb·CO(g),实验表明,Hb·CO的浓度即使只有Hb·O2浓度的2%,足以使人的智力受损,试回答: ①上述反应的平衡常数表达式为K=___。 ②已知37℃时,该反应平衡常数K=220,抽烟后,测得吸入肺部的空气中的CO和O2的浓度分别为1×10-6 mol/L和1×10-2mol/L,能否使人的智力受损____(填“能”或“否”),理由是___。