
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
| C2(SO3) |
| C2(SO2)Ј®C(O2) |
| C2(SO3) |
| C2(SO2)Ј®C(O2) |
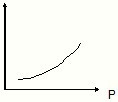 ҪУҙҘ·ЁЦЖБтЛб№ӨТХЦРЈ¬ЖдЦч·ҙУҰФЪ450ЎжІўУРҙЯ»ҜјБҙжФЪПВҪшРРЈә
ҪУҙҘ·ЁЦЖБтЛб№ӨТХЦРЈ¬ЖдЦч·ҙУҰФЪ450ЎжІўУРҙЯ»ҜјБҙжФЪПВҪшРРЈә| С№ЗҝЧӘ»ҜВКОВ¶И | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400Ўж | 99.2% | 99.6% | 99.7% | 99.9% |
| 500Ўж | 93.5% | 96.9% | 97.8% | 99.3% |
| 600Ўж | 73.7% | 85.8% | 89.5% | 96.4% |
 ·ЦұрұнКҫSO3ЧӘ»ҜіЙЙПКцБҪЦЦБтЛбКұЈ¬УГЛ®өДЦКБҝУлSO3ОпЦКөДБҝөД№ШПөКҪ·ЦұрКЗЈә
·ЦұрұнКҫSO3ЧӘ»ҜіЙЙПКцБҪЦЦБтЛбКұЈ¬УГЛ®өДЦКБҝУлSO3ОпЦКөДБҝөД№ШПөКҪ·ЦұрКЗЈә =______
=______ Ј¬
Ј¬ =______
=______ Ј»
Ј» Ј¬
Ј¬ өДБтЛбөДЦКБҝЈ¬
өДБтЛбөДЦКБҝЈ¬ өД·ўСМБтЛбөДЦКБҝЈ©Ул
өД·ўСМБтЛбөДЦКБҝЈ©Ул УГБҝЦ®ұИөД№ШПөКЗЈә
УГБҝЦ®ұИөД№ШПөКЗЈә ___________xЈ»
___________xЈ» өДОпЦКөДБҝТ»¶ЁЈ¬xЛжКРіЎРиЗу¶шУРёДұдЈ¬ФтУГЛ®ЧЬБҝ
өДОпЦКөДБҝТ»¶ЁЈ¬xЛжКРіЎРиЗу¶шУРёДұдЈ¬ФтУГЛ®ЧЬБҝ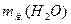 ЎўxЎў
ЎўxЎў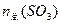 өД№ШПөКҪКЗ_________________ЎЈ
өД№ШПөКҪКЗ_________________ЎЈ°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com