
题目列表(包括答案和解析)
将下列物质进行分类:
①11H与13H;②O2与O3;③乙醇与甲醚(CH3-O-CH3);④H2O与D2O;⑤CH3CH2CH2CH3与CH3-CH(CH3)-CH3;⑥C60与C70;⑦CH4与C4H10
(1)互为同位素的是 (填编号,下同);互为同素异形体的是
互为同分异构体的是 互为同系物的是
(2)有下列反应:①由乙烯制乙醇;②甲烷在空气中燃烧;③由乙烯制氯乙烷;④丙烯使溴水褪色;⑤苯与浓硝酸、浓硫酸的混合酸反应;⑥用丙烯制聚丙烯;其中属于取代反应的是(填序号,下同) ,属于氧化反应的是 ,属于加成反应的是 ,属于加聚反应的是 。
(3)①正丁烷;②异丁烷;③正戊烷;④异戊烷;⑤新戊烷;⑥丙烷,物质的沸点由高到低的排列顺序是:
(4)某学生用0.100 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3 cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是(用序号字母填写)__________________________________。
(14分) 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:?
(1)以天然气为原料制H2是合成氨的一条重要的路线。甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:
①CH (g)+1/2O
(g)+1/2O (g)=CO(g)+2H
(g)=CO(g)+2H (g)
(g)  H1=-35.6kJ·mol
H1=-35.6kJ·mol
试判断常温下,上述反应能否自发进行: (填”能”或”否”)。有研究认为甲烷部分氧化的机理为:
②CH (g)+2O
(g)+2O (g)=CO2(g)+2H2O(g)
(g)=CO2(g)+2H2O(g)  H2=-890.3kJ·mol
H2=-890.3kJ·mol
③CH (g)+CO
(g)+CO (g)=2CO(g)+2H
(g)=2CO(g)+2H (g)
(g)  H3=247.3kJ·mol
H3=247.3kJ·mol
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:
。
⑵恒温下,向一个2L的密闭容器中充入1 molN2和2.6 molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
实验数据
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/( mol ·/L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

 的物质的量浓度 。
的物质的量浓度 。氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: CH4(g)+H2O(g)==== CO (g)+3H2(g)![]() H= +206.2 kJ·mol-1
H= +206.2 kJ·mol-1
CH4(g)+ CO2(g)==== 2CO(g)+2H2(g) 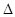 H = +247.4 kJ·mol-1
H = +247.4 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______________________________。
(2)电解尿素[CO(NH)]的碱性溶液制氢的装置示意图见图:
(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极排出液中含有大量的碳酸盐成份,则阳极的电极反应式为_______,每消耗1mol尿素需要补充______mol氢氧化钾。
(14分) 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:?
(1)以天然气为原料制H2是合成氨的一条重要的路线。甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:
①CH(g)+1/2O
(g)=CO(g)+2H
(g)
H1=-35.6kJ·mol
试判断常温下,上述反应能否自发进行: (填”能”或”否”)。有研究认为甲烷部分氧化的机理为:
②CH(g)+2O
(g)=CO2(g)+2H2O(g)
H2=-890.3kJ·mol
③CH(g)+CO
(g)=2CO(g)+2H
(g)
H3=247.3kJ·mol
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:
。
⑵恒温下,向一个2L的密闭容器中充入1molN2和2.6 molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
实验数据
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/( mol ·/L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
此条件下,该反应达到化学平衡时,氮气的浓度为 。
(3)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。?
①b处电极上发生的电极反应式是 。
②电镀结束后,装置Ⅰ中溶液的pH (填写“变大”、“变小”或“不变”,下同),装置Ⅱ中Cu的物质的量浓度 。
③若完全反应后,装置Ⅱ中阴极质量增加12.8g,则装置Ⅰ中理论上消耗甲烷 L (标准状况下)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com