
题目列表(包括答案和解析)
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的某种原子没有中子;Y与X相邻,Y与Z也相邻,X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高。 试回答下列问题:
(1)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,写出其中两种离子发生反应生成其中两种分子的离子方程式 。
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A和B是日常生活中常用调味品的主要成分,且A与B能够反应生成C,试写出该反应化学方程式 。
(3)由W、X、Y、Z四种元素的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式 。
(4)由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如右图所示的转化关系。
①写出A与B反应生成C的化学方程式 。

②向50mL 4mol·L-1的NaOH溶液中通入1.12L气体B(标准状况),反应后溶液中溶质的物质的量之比为
。
(5)W、Y、Z三种元素可组成一种无机盐,其组成可表示为W4Y2Z3。该盐溶液中离子浓度由大到小的顺序为 。
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高.试回答下列各题:
(1)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,写出其中两种离子发生反应生成两种分子的离子方程式________.
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A是日常生活中常用调味品的主要成分,且A与B能够反应生成C,C是一种有香味的液体.试写出该反应的化学方程________
(3)由W、X、Y、Z四种元素中的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式________.
(4)已知由元素X和Z可组成A、B、C、D四种中学化学中常见的单质或化合物,四种物质之间存在如图所示的转化关系.
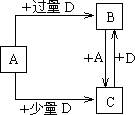
①写出A与B反应生成C的化学方程式________;
②向50 mL 4 mol·L-1的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中溶质的物质的量之比为________.
(5)W、Y、Z三种元素可组成一种无机盐,其组成可表示为W4Y2Z3,则该溶液中离子浓度由大到小的顺序为________.
已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.

(1)如果A、B是10电子离子,C、D是10电子分子,
A、B、C、D均含有两种元素.请写出A、B的电子式:
A 、B 、C、D的化学式 C 、D .
(2)写出A离子与B反应的离子方程式: .
(10分)水是生命之源,也是化学反应中的主角。请回答下列问题:(下列问题
所涉及的答案可能有多种,只需答出一种情况即可)
I.水是一种电解质,发生电离会产生电子总数相同的两种微粒,其电离的方程式为
。
Ⅱ.有以下五组离子① K+、Cl-、NO3-、S2- ;② K+、Fe2+、I-、SO42- ;③ Na+、Cl-、
NO3-、SO42-;④Na+、Ca2+、Cl-、HCO3-;⑤ K+、Ba2+、Cl-、NO3-。在由水电离产生的
c(OHˉ)= 1×10ˉ13mol/L溶液中,一定不能大量共存的离子组是 (填序号)
Ⅲ.在许多反应中H2O扮演不同的“角色”。请结合所学完成下列反应
(1)H2O参与的置换反应:符合X+W→Y+V,已知X和Y分别是短周期同主族两种元素形成的单质, W、V是化合物
①W是水,离子方程式为 ;
②V是水,化学方程式为 。
(2)水既不是氧化剂也不是还原剂的氧化还原反应:
A、B是中学化学常见的两种由短周期元素组成的有色气体,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,写出A、B与水反应的化学方程式:
①A + H2O ;
②B + H2O ;
(10分)水是生命之源,也是化学反应中的主角。请回答下列问题:(下列问题
所涉及的答案可能有多种,只需答出一种情况即可)
I.水是一种电解质,发生电离会产生电子总数相同的两种微粒,其电离的方程式为
。
Ⅱ.有以下五组离子① K+、Cl-、NO3-、S2- ;② K+、Fe2+、I-、SO42- ;③ Na+、Cl-、
NO3-、SO42- ; ④Na+、Ca2+、Cl-、HCO3- ;⑤ K+、Ba2+、Cl-、NO3-。在由水电离产生的
c(OHˉ)= 1×10ˉ13mol/L溶液中,一定不能大量共存的离子组是 (填序号)
Ⅲ.在许多反应中H2O扮演不同的“角色”。请结合所学完成下列反应
(1)H2O参与的置换反应:符合X+W→Y+V,已知X和Y分别是短周期同主族两种元素形成的单质, W、V是化合物
①W是水 ,离子方程式为 ;
②V是水, 化学方程式为 。
(2)水既不是氧化剂也不是还原剂的氧化还原反应:
A、B是中学化学常见的两种由短周期元素组成的有色气体,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,写出A、B与水反应的化学方程式:
①A + H2O ;
②B + H2O ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com