
题目列表(包括答案和解析)
(12分)为了测定m g氢氧化钠和碳酸钠的固体混合物中碳酸钠的质量分数,甲、乙
![]() 两位同学分别设计了如下的实验方案:
两位同学分别设计了如下的实验方案:
(1)甲同学的方案是:将样品溶解,加入过量氯化钡溶液,过滤、洗涤,取沉淀烘干,称量得固体ng。则混合物中碳酸钠的质量分数为 ;
(2)乙同学的方案是:将样品溶解后,加入稍过量的氯化钡溶液,再滴入2―3滴酚酞试液,用标准盐酸滴定。乙同学在滴定过程中所需要的主要玻璃仪器有 、 。加入过量氯化钡溶液的目的是 。

(3)丙同学的方案如下图所示当混合物样品完全反应时,缓慢通入空气的目的是 ,其中,装置A的作用是 ,装置E的作用 。
为了测定m g氢氧化钠和碳酸钠的固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
(1)甲同学的方案是:将样品溶解,加入过量氯化钡溶液,过滤、洗涤,取沉淀烘干,称量得固体ng.则混合物中碳酸钠的质量分数为________;
(2)乙同学的方案是:将样品溶解后,加入稍过量的氯化钡溶液,再滴入2-3滴酚酞试液,用标准盐酸滴定.乙同学在滴定过程中所需要的主要玻璃仪器有________、________.加入过量氯化钡溶液的目的是________.
(3)丙同学的方案如下图所示
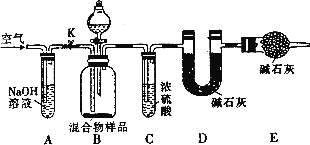
当混合物样品完全反应时,缓慢通入空气的目的是________,其中,装置A的作用是________,装置E的作用________.
为了测定氢氧化钠固体混合物m g中碳酸钠的质量分数,某探究活动小组分别设计了如下实验方案:
(1)甲同学用如图一所示装置,通过测定放出CO2的体积来确定碳酸钠的质量分数,结果误差较大,请你提出改进措施 ;
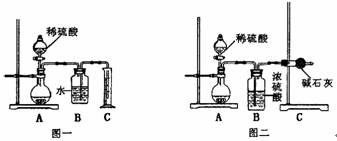
(2)乙同学用图二所示装置,通过测定反应放出CO2的质量来确定碳酸钠的质量分数,他重复正确操作三次,结果数据出现了较大偏差。你认为主要原因可能是(任写两个)
①
②
(3)丙同学认为上面的测定方法误差都较大,提出用中和滴定来测定。方法是:准确称取氢氧化钠样品m g,放入锥形瓶中加蒸馏水溶解,加1―2滴酚酞指示剂,用物质的量浓度为c mol?L―1的HCl溶液滴定至溶液由红色至无色(指示CO32―+H+=HCO3―反应的终点),消耗HCl溶液体积为V1mL,再加入1―2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙(指示H++HCO3―=CO2↑+H2O反应的终点),又消耗HCl溶液体积为V2ml。则烧碱样品中Na2CO3的质量分数为 ;
(4)请你设计另外一个简单的实验方案来测定NaOH固体混合物中Na2CO3的质量分数。
①写出操作步骤
②用测得的数据(用字母表示)写出质量分数的表达式 。
(10分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀_________(填操作步骤)、洗涤、烘干、称量。洗涤沉淀的操作是________________________________。
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应后,用如图装置测
定产生CO2气体的体积,为了测定结果准确,B中
的溶液最好采用____________,从下列各选项中选
取:
a.饱和碳酸钠溶液 b.饱和碳酸碳酸氢钠溶液.
c.饱和氢氧化钠溶液 d.饱和硫酸铜溶液。
若直接采用如图装置, 选用该溶液后实验结果仍
然不够准确,其原因可能是________________________________________。
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口瓶中 ③检验装置的气密性。④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打并止水夹 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟。
I.正确的操作顺序是(填写序号):
③→_______→⑥→________→⑤→_______→⑦→__________→④
Ⅱ.若去掉装置A,测定结果___________;若去掉装置B,测定结果__________(填“偏大”、“偏小”或“无影响”).
(10分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀_________(填操作步骤)、洗涤、烘干、称量。洗涤沉淀的操作是________________________________。
方案二:气体分析法
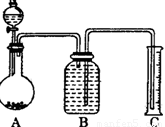
(2)把一定量的样品与足量盐酸反应后,用如图装置测
定产生CO2气体的体积,为了测定结果准确,B中
的溶液最好采用____________,从下列各选项中选
取:
a.饱和碳酸钠溶液 b.饱和碳酸碳酸氢钠溶液.
c.饱和氢氧化钠溶液 d.饱和硫酸铜溶液。
若直接采用如图装置, 选用该溶液后实验结果仍
然不够准确,其原因可能是________________________________________。
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口瓶中 ③检验装置的气密性。④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打并止水夹 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟。
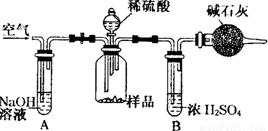
I.正确的操作顺序是(填写序号):
③→_______→⑥→________→⑤→_______→⑦→__________→④
Ⅱ.若去掉装置A,测定结果___________;若去掉装置B,测定结果__________(填“偏大”、“偏小”或“无影响”).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com