
题目列表(包括答案和解析)
右图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
![]()
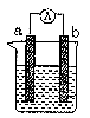 (1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
![]() (2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,![]() 该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极
该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极
![]() (3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。
![]() 现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解
现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解![]() 液;
液;
甲烷应通入 极(填a或b,下同),电子从 极流出。
右图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
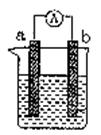
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入 极(填a或b,下同),电子从 极流出。a极发生电极反应式为:_________________________
(9分) 右图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: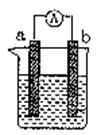
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置 (填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请指出正、负极
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用酸性溶液为电解液;则氢气应通入 极(填a或b,下同),电子从 极流出。a极发生电极反应式为:_________________________
| ||

| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol?L-1 H2SO4至溶液显酸性,然后将所得溶液分置于A、B试管中. | / |
| 步骤2: | |
| 步骤3: |
 2CaSO4+2Cl2↑+2H2O.以下是制取CI2并验证其部分性质的实验装置.
2CaSO4+2Cl2↑+2H2O.以下是制取CI2并验证其部分性质的实验装置.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3mol?L-1 H2SO4至溶液显酸性,然后将所得溶液分置于A、B试管中. | |
| 步骤2: | |
| 步骤3: |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com