
题目列表(包括答案和解析)
下列有关氨的性质的叙述中,正确的是
A.氨水是一种弱电解质
B.氨气和酸都能在空气中相遇产生白色烟雾
C.液氨常用来做致冷剂
D.氨的分子结构呈正四面体,是非极性分子
(08厦门市质检)在元素周期表中相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等。运送飞船的火箭燃料有一种液态氮氢化合物。已知该化合物的相对分子质量为32,其中氢元素的质量分数为12.5%,分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子式为 ,其沸点比氨__________ (填“高”或“低”),稳定性比氨__________ ( 填“好”或“差”)。
(2)若64g该氮氢化合物与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量。试写出该反应的热化学方程式: 。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl NH4Cl。试写出上述氮氢化合物加入足量盐酸时,发生反应的化学方程式为 。
(4)氮原子间也可形成链状结构,假设氮原子间只以N-N键形式连接,并形成氢化物,则该系列氢化物的通式为 。
 (2013?盐城一模)[物质结构与性质]
(2013?盐城一模)[物质结构与性质]| H | - 4 |
| 储氢 |
| 输氢 |
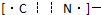
| 52 |
| a.NA |
| 52 |
| a.NA |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com