
题目列表(包括答案和解析)
溶液 | KOH | HNO3 | CH3COOH | HCl |
溶质质量分数w(%) | 56 | 63 | 60 | 36.5 |
物质的量浓度c(mol·L-1) | 14.3 | 13.8 | 10.6 | 11.8 |
根据表中数据判断上述四种溶液中的密度最小的是
A.HCl B.HNO
用下图所示装置进行实验可以研究CO的还原性.

填写下列空白:
(1)从A的长颈漏斗应加入的试剂是________.(填序号)
①稀H2SO4
②浓H2SO4
③稀HCl
④浓HNO3
(2)装置B中最适宜的试剂是________
(3)装置D中发生的化学方程式是________.
(4)装置E中发生的现象是________.
(5)必须用装置C吸收水蒸气的主要原因是________.
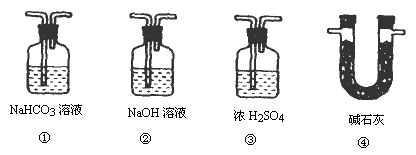
(6)若根据F中石灰水变浑浊的现象也能确认CO具有还原性,应在上图装置________与________之间连接下图中的________装置.

| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② H2CO3或H2SO4、H2SO3、H2S、HNO3、HNO2 H2CO3或H2SO4、H2SO3、H2S、HNO3、HNO2 |
③ KOH或NaOH KOH或NaOH ④Ba(OH)2 |
⑤Na2CO3 ⑥ K2CO3或K2S、K2SO3、K2SO4、KNO3、KNO2、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2 K2CO3或K2S、K2SO3、K2SO4、KNO3、KNO2、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2 |
⑦CO2 ⑧Na2O |
⑨NH3 ⑩H2O2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com