
题目列表(包括答案和解析)
(11分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。
C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______________。
(3)CaTiO3晶体中(晶胞结构如图所示),Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______; 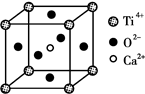
(11分)研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。
C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 每个COCl2分子内含有
个δ键, 个π键。其中心原子采取 杂化轨道方式。
每个COCl2分子内含有
个δ键, 个π键。其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______________。
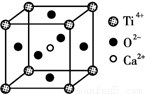
(3)CaTiO3晶体中(晶胞结构如图所示) ,Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______;
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是__________________________________________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
![]() ①COCl2分子的结构式为 每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
①COCl2分子的结构式为 每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
 ②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。
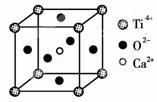
(3)CaTiO3晶体中(晶胞结构如图所示)
晶体中,Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______;
指出下列哪些是碳链异构___________;哪些是位置异构_________ _____;哪些是官能团异构___________ __。
| A.CH3CH2COOH | B.CH3-CH(CH3)-CH3 | C.CH2=CH-CH=CH2 | D.CH3COOCH3 E.CH3-CH2-C≡CH F.HCOOCH2CH3 |
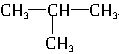 和CH3CH2CH2CH3:________;
和CH3CH2CH2CH3:________;湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com