
题目列表(包括答案和解析)
短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):
(1)Y在周期表的位置是______________________ _;Z2的结构式是________________。
(2)反应①的离子方程式是______________________________________________________。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去)。
Ⅰ、 写出反应②的离子方程式__________________ ___________。
II、上述实验装置不够完善,改进方法是 。
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是 。
短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):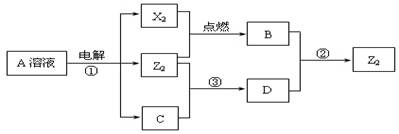
(1)Y在周期表的位置是______________________ _;Z2的结构式是________________。
(2)反应①的离子方程式是______________________________________________________。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去)。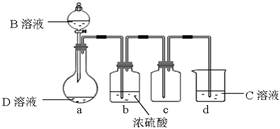
Ⅰ、写出反应②的离子方程式__________________ ___________。
II、上述实验装置不够完善,改进方法是 。
Ⅲ、足量Z2通入FeBr2溶液中发生反应的离子方程式是 。
短周期元素X、Y、Z的原子序数依次增大,其原子的最外层电子电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍;下列说法正确的是 ( )
A.X的最高价氧化物对应的水化物显弱酸性
B.X的氢化物的水溶液在空气中存放不易变质
C.Y的氧化物是离子化合物
D.X的氢化物和Z的氢化物反应生成一种对热稳定的化合物
短周期元素X、Y、Z的原子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):

(1)Y在周期表的位置是______________________ _;Z2的结构式是________________。
(2)反应①的离子方程式是______________________________________________________。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如下图所示(夹持固定装置的仪器已略去)。

Ⅰ、 写出反应②的离子方程式__________________ ___________。
II、上述实验装置不够完善,改进方法是 。
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com