
题目列表(包括答案和解析)
| 现象 | 解释 | |
| A | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物溶于浓硝酸 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成. | 淀粉没有水解成葡萄糖 |
| C | 铜片放入浓硫酸中,无明显变化 | 说明铜在冷的浓硫酸中发生钝化 |
| D | KI淀粉溶液中通入Cl2,溶液变蓝 | KI被Cl2氧化后生成的I2与淀粉发生显色反应 |
| A、A | B、B | C、C | D、D |
在做铜与浓、稀硝酸反应的实验时,化学活动小组的同学观察到奇妙的速率变化:铜与稀硝酸反应时“开始较慢,一段时间后有所加快,后又减慢”,而铜与浓硝酸反应时“开始较慢,至
30 s左右突然加快”.随后活动小组的同学对铜与浓硝酸反应时“开始较慢,至30 s左右突然加快”这一现象的原因展开了探讨.(1)分别写出Cu与浓HNO3、稀HNO3反应的离子方程式:________、________.
(2)甲认为可能是铜与浓硝酸反应放热使溶液温度升高所致,乙同学通过对实验现象进行认真分析后否定了这一说法,他的理由是________.
(3)请你根据所学的知识作出合理猜想并设计实验证明.你的猜想是________,你的实验设计是________.
某同学在学习硝酸与硫酸时,对两种酸与铜的反应情况进行研究,试完成下列各题。
(1)在甲、乙两个烧杯中,分别装入40mL浓度均为2mol·L-1的稀硫酸和稀硝酸,并向其中各加入 4g束状铜丝,观察现象,试完成下列实验报告:

(2)充分反应后,将甲、乙烧杯混合,再使之充分反应,最终所得溶液溶质为____ ,剩余固体总质量为 g
(3)若甲中硫酸溶液体积V(V>40mL)可变,其余数据不变,则:
①当甲、乙烧杯混合充分反应后,溶液中只有一种溶质时,V=____ mL,若要将溶液中的Cu2+沉淀完全,应加NaOH使溶液的pH至少为____
。已知KsP[Cu(OH)2]=2.2×l0-20,1g  =0.7)
=0.7)
②能否通过硫酸溶液体积的改变,使铜丝在甲、乙烧杯混合充分反应后完全溶解? 试写出推理过程________ 。
某同学在学习硝酸与硫酸时,对两种酸与铜的反应情况进行研究,试完成下列各题。
(1)在甲、乙两个烧杯中,分别装入40mL浓度均为2mol·L-1的稀硫酸和稀硝酸,并向其中各加入 4g束状铜丝,观察现象,试完成下列实验报告: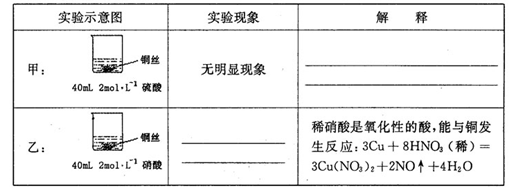
(2)充分反应后,将甲、乙烧杯混合,再使之充分反应,最终所得溶液溶质为____ ,剩余固体总质量为 g
(3)若甲中硫酸溶液体积V(V>40mL)可变,其余数据不变,则:
①当甲、乙烧杯混合充分反应后,溶液中只有一种溶质时,V=____ mL,若要将溶液中的Cu2+沉淀完全,应加NaOH使溶液的pH至少为____ 。已知KsP[Cu(OH)2]=2.2×l0-20,1g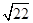 =0.7)
=0.7)
②能否通过硫酸溶液体积的改变,使铜丝在甲、乙烧杯混合充分反应后完全溶解? 试写出推理过程________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com