无水AlCl
3可用作有机合成的催化剂、食品膨松剂等.工业制备无水AlCl
3的流程如下:
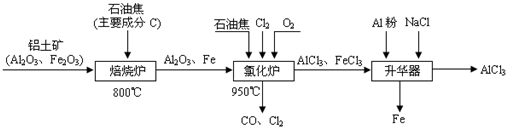
(1)已知:C(s)+
O
2(g)═CO(g)△H=-110.5kJ/mol,2Fe(s)+
O
2(g)═Fe
2O
3(s)△H=-822.1kJ/mol
请写出C还原Fe
2O
3生成CO的热化学方程式
3C(s)+Fe2O3(s)═3CO(g)+2Fe(s)△H=+490.6kJ/mol
3C(s)+Fe2O3(s)═3CO(g)+2Fe(s)△H=+490.6kJ/mol
.
(2)反应2CO+O
2
2CO
2的平衡常数为K
1;反应4Fe+3O
2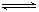
2Fe
2O
3的平衡常数K
2,则反应3CO+Fe
2O
3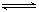
2Fe+3CO
2的平衡常数K与K
1、K
2的关系式
.
(3)高温下,氧化铁能跟碳发生下列反应:
①Fe
2O
3+3C
2Fe+3CO ②Fe
2O
3+3CO
2Fe+3CO
2若反应产生的气体是CO
2和CO,则
的取值范围是
.
(4)氯化炉中生成的气体,通常用碱性的亚硫酸钠溶液来吸收,请用离子方程式分析亚硫酸钠溶液呈碱性的原因
SO
32-+H
2O
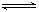
HSO
3-+OH
-SO
32-+H
2O
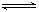
HSO
3-+OH
-.
(5)氯化炉中发生:3Cl
2(g)+3C(s)+Al
2O
3(s)
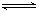
2AlCl
3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是
①⑤
①⑤
(填序号):
①增加C的量 ②多通入Cl
2③升高温度 ④移走部分AlCl
3(g) ⑤使用合适的催化剂工业上还常采用向氯化炉中通入O
2的方法,其目的是
与C或CO反应,提供反应所需的热量
与C或CO反应,提供反应所需的热量
.
(6)沉淀分析法一般规定:溶液中某离子物质的量浓度低于1.0×10
-5mol/L时,可认为已沉淀完全.现向一定浓度的AlCl
3和FeCl
3的混合溶液中逐滴加入氨水,当Fe
3+完全沉淀时,测定c(Al
3+)=0.2mol/L.此时所得沉淀中
否
否
(填“是”或“否”)含有Al(OH)
3.(已知:Ksp[Fe(OH)
3]=4.0×10
-38,Ksp[Al(OH)
3]=1.1×10
-33).


 2CO2的平衡常数为K1;反应4Fe+3O2
2CO2的平衡常数为K1;反应4Fe+3O2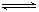 2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3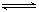 2Fe+3CO2的平衡常数K与K1、K2的关系式
2Fe+3CO2的平衡常数K与K1、K2的关系式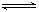 HSO3-+OH-
HSO3-+OH-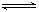 HSO3-+OH-
HSO3-+OH-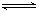 2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是
2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是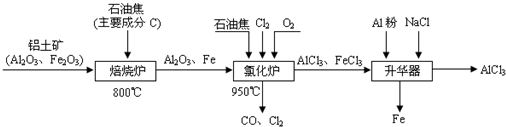
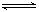
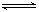
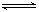
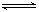
 4NO+6H2O
4NO+6H2O CaSiO3
CaSiO3 2Fe+3CO
2Fe+3CO