
题目列表(包括答案和解析)
下列离子方程式与所述事实相符且正确的是( )
①将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO-
②漂白粉溶液在空气中失效:ClO-+CO2+H2O===HClO+HCO3-
③向Na[Al(OH)4]溶液中通入过量CO2制Al(OH)3:[Al(OH)4]-+CO2===Al(OH)3↓+HCO3-
④将铁粉加入稀H2SO4中:2Fe+6H+===2Fe3++3H2↑
⑤用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-===Mn2++Cl2↑+2H2O
⑥用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2===2Mn2++5O2↑+8H2O
A.③⑥ B.⑤⑥ C.①② D.③
(8分)某科研小组,用含有少量的CaO和Fe2O3的高岭土(主要成分:Al2O3·2SiO2·2H2O)来研制新型净水剂,其实验方案如下:将土样和纯碱混合均匀,加热熔融,冷却后用水浸取熔块,过滤弃去残渣,滤液用盐酸酸化,经过滤,分别得到沉淀和溶液,溶液即是净水剂。
(1)土样和纯碱混合均匀,加热熔融时,土样中的主要成分与纯碱反应的化学方程式为:
① ;②Al2O3+Na2CO3 2NaAlO2+CO2↑。
2NaAlO2+CO2↑。
(提示:NaAlO2易溶于水并转化为Na[Al (OH)4])
(2)最后得到的沉淀物是 ,生成沉淀的离子方程式为 。
(3)实验室中常备的坩埚有瓷坩埚,氧化铝坩埚和铁坩埚,本实验熔融土样时应选用 坩埚。
(8分)某科研小组,用含有少量的CaO和Fe2O3的高岭土(主要成分:Al2O3·2SiO2·2H2O)来研制新型净水剂,其实验方案如下:将土样和纯碱混合均匀,加热熔融,冷却后用水浸取熔块,过滤弃去残渣,滤液用盐酸酸化,经过滤,分别得到沉淀和溶液,溶液即是净水剂。
(1)土样和纯碱混合均匀,加热熔融时,土样中的主要成分与纯碱反应的化学方程式为:
① ;②Al2O3+Na2CO3![]() 2NaAlO2+CO2↑。
2NaAlO2+CO2↑。
(提示:NaAlO2易溶于水并转化为Na[Al (OH)4])
(2)最后得到的沉淀物是 ,生成沉淀的离子方程式为 。
(3)实验室中常备的坩埚有瓷坩埚,氧化铝坩埚和铁坩埚,本实验熔融土样时应选用 坩埚。
下列物质间的转化在给定条件下能够实现的是( )
①Al2O3 NaAlO2(aq)或Na[Al(OH)4](aq)
NaAlO2(aq)或Na[Al(OH)4](aq)
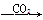 Al(OH)3
Al(OH)3
②S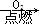 SO3
SO3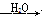 H2SO4
H2SO4
③NaOH(aq)  NaHCO3
NaHCO3 Na2CO3
Na2CO3
④Fe2O3 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3
⑤NH4Cl(s)  NH3
NH3 NH4HCO3
NH4HCO3
A. ①③⑤ B. ②③④ C. ②④⑤ D. ①④⑤
下列不属于配合物的是( )
| A.[Cu(H2O)4]SO4·H2O | B.[Ag(NH3)2]OH |
| C.KAl(SO4)2·12H2O | D.Na[Al(OH)4] |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com