(2013?房山区一模)某黄铜矿样品标注显示:主要成分为CuFeS
2(含81.5%),其余多为脉石(SiO
2).为检验该黄铜矿的纯度是否与标注一致,设计了如下实验:
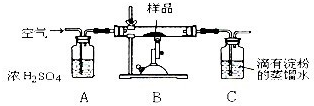
已知:①在空气存在下煅烧黄铜矿,生成Cu、Fe
3O
4和SO
2气体.②亚硫酸易被氧化:2H
2SO
3+O
2=2H
2SO
4请回答下列问题:
(1)检验装置气密性后,称取研细的黄铜矿样品1.150g,放入硬质玻璃管中,研细的目的是
使样品快速、充分反应
使样品快速、充分反应
.
(2)通入空气一段时间后,点燃酒精喷灯加热样品,充分反应,装置B、装置C中反应的化学方程式分别是
3CuFeS
2+8O
23Cu+Fe
3O
4+6SO
23CuFeS
2+8O
23Cu+Fe
3O
4+6SO
2、
SO2+H2O?H2SO3
SO2+H2O?H2SO3
.
(3)反应过程中,装置A的作用是
②④
②④
(填序号).
①除去空气中的二氧化碳 ②除去空气中的水蒸气 ③使空气成分均匀混合 ④用于观察、控制空气流速
(4)反应结束前的操作是:先撤掉酒精喷灯,再
通入空气至硬质玻璃管冷却
通入空气至硬质玻璃管冷却
,其目的是
防止C中溶液倒吸且使装置内SO2被C溶液充分吸收反应
防止C中溶液倒吸且使装置内SO2被C溶液充分吸收反应
.
(5)取装置C中溶液的1/10置于锥形瓶中,用0.05mol?L
-1标准碘溶液进行滴定,反应的离子方程式为
I2+H2SO3=SO42-+2I-
I2+H2SO3=SO42-+2I-
;判断滴定达到终点的现象是
无色溶液变蓝色
无色溶液变蓝色
;若滴定中消耗标准碘溶液20.00mL,则该黄铜矿的纯度测定结果比标注值
偏低
偏低
(偏低或偏高),造成该结果的原因之一可能是
SO2与H2O反应可逆致少量SO2跑掉或H2SO3易被氧化
SO2与H2O反应可逆致少量SO2跑掉或H2SO3易被氧化
,改进的建议是
减慢通入空气的速度或改用NaOH淀粉溶液吸收SO2
减慢通入空气的速度或改用NaOH淀粉溶液吸收SO2
.

