
题目列表(包括答案和解析)
| ||
| ||
| ||
| ||
| ||
| ||
A是一种常见的烃,标准状况下,A对氢气的相对密度是14。乳酸是一种常见的有机酸,用途广泛。高吸水性树脂F是一种高分子材料,可用于干旱地区抗旱保水、改良土壤、改造沙漠,还可制作尿不湿。下图是由A为原料制取高吸水性树脂F的合成路线图:
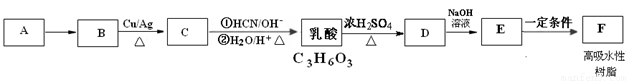
已知: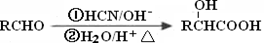
请回答:
(1)A的名称是
,A B的反应类型是
。乳酸中的官能团名称为
B的反应类型是
。乳酸中的官能团名称为
(2)B  C的化学方程式是
。
C的化学方程式是
。
乳酸 D的化学方程式为
D的化学方程式为
(3)乳酸分子中核磁共振氢谱峰面积比是 。乳酸有多种同分异构体,其中所含官能团与乳酸相同的为 (用结构简式表示)
(4)一定条件下,乳酸经聚合可制得聚乳酸,聚乳酸在医疗上可做手术缝合线,聚乳酸的结构简式为
(5)F的结构简式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com