
题目列表(包括答案和解析)
(1)A、B、C各是什么元素,并画出它们的原子结构示意图。?
(2)比较A和B的最高价氧化物的酸性强弱,并举一个具体反应加以说明。?
(3)排出A、B、C原子半径由小到大的顺序。?
(4)写出B的氢化物在空气中自燃的化学方程式,并注明电子得失的方向和数目。?
| A.B3A2分子晶体 | B.BA2原子晶体 |
| C.A3B2离子晶体 | D.AB2原子晶体 |
(14分)某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:
甲 + 乙丙 + 丁 + 水。
(1)若丙为NO2。
①甲与乙反应的化学方程式为 。
②火箭常用NO2的二聚体N2O4作氧化剂,肼(N2H4)作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H =-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)N2O4(g) △H =-52.7kJ·mol-1
试写出气态肼(N2H4)在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
___________________________________________________。
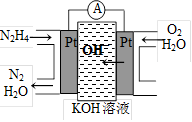
③肼又称联氨,广泛用于火箭推进剂、有机合成及燃料电池。肼燃料电池原理如右图所示,右边电极为 (填“正极”、“负极”),左边电极上发生的电极反应式为 。
(2)若丙为SO2。
①把乙滴入硫酸铜晶体中,观察到的现象是 。
②SO2气体有毒,多余的SO2气体常用足量的NaOH溶液吸收,写出吸收液中离子浓度由大到小的顺序: 。
③在氧化还原反应的过程中,氧化反应和还原反应同时发生,有关反应:
SO2-2e-+2H2O =SO42-+4H+反应的说法错误的是 。
A.该反应为氧化反应
B.上述反应中若转移电子物质的量为0.05mol,则生成溶液的PH值为1
C.Fe2(SO4)3、品红两种溶液都能使上述反应进行
D.通入Cl2会降低SO2的漂白作用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com