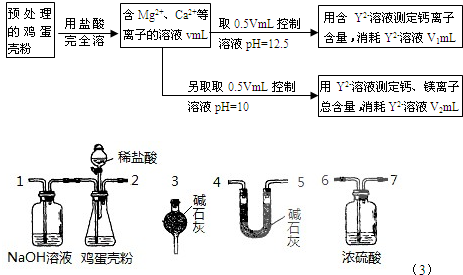
(2010?龙岩模拟)鸡蛋壳中含有大量钙、少量镁和钾等元素.实验室可用图示流程测定鸡蛋壳中钙、镁元素含量.依据的反应可以表示为:Ca
2++Y
2-=CaY、Mg
2++Y
2-=MgY.回答下列问题.
(1)测定Ca
2+、Mg
2+总含量时,控制溶液pH=10.若pH过大,测定结果将
偏小
偏小
(填“偏大”、“偏小”或“无影响”);
(2)测定Ca
2+含量的关键是控制溶液的pH,使溶液中Mg
2+形成沉淀,若要使溶液中c(Mg
2+)不大于1.2×10
-7mol/L,则溶液pH应不小于
12
12
(已知:ksp[Mg(OH)
2]=1.2×10
-11,上述实验均在室温下进行).
(3)如果鸡蛋壳粉质量为mg,溶液中Y
2+浓度为c mol/L,则鸡蛋壳样品中镁元素质量分数是
.
(4)有同学提出可采用如右装置、通过测定鸡蛋壳与盐酸反应产生的二氧化碳的量就能测定鸡蛋壳中的钙的总含量.
①采用该方法进行实验,各装置从左到右的连接顺序依次1-2-
6-7-4-5-3或6-7-5-4-3
6-7-4-5-3或6-7-5-4-3
(填各装置对应接口的数字序号).
②若排除实验仪器和操作的影响因素,此实验方法测得的结果是否准确?
答:
不一定准确
不一定准确
(填“准确”、“不准确”或“无法判断”).原因是
如果蛋壳中钙元素全部以碳酸钙形式存在,且不再含有能与盐酸反应产生酸性气体的其他物质,则测定结果准确;否则不准确
如果蛋壳中钙元素全部以碳酸钙形式存在,且不再含有能与盐酸反应产生酸性气体的其他物质,则测定结果准确;否则不准确
.

 (2010?安徽模拟)维生素C又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品和饮料的添加剂(如苹果汁等),其结构如图.下列有关说法正确的是( )
(2010?安徽模拟)维生素C又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品和饮料的添加剂(如苹果汁等),其结构如图.下列有关说法正确的是( )
