
题目列表(包括答案和解析)
(07年山东卷)(8分)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
 |
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是______。电解槽中的阳极材料为__________ 。
(2)本工艺流程中先后制得Br2、 CaSO4 和Mg(OH)2,能否按Br2、Mg(OH)2、 CaSO4 的顺序制备?____ ,原因是_____。
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是_______ 。
(08年山东卷)(16分)食盐是日常生活的必需品,也是重要的化工原料。
⑴粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
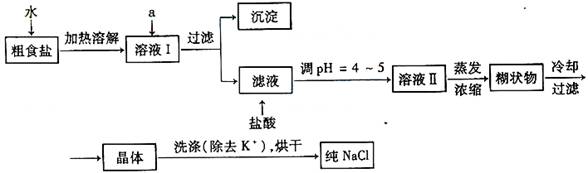
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为 _____ (只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_____ 。
 ⑵用提纯的NaCl配制500mL4.00 mol?L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有 ______ (填仪器名称)。
⑵用提纯的NaCl配制500mL4.00 mol?L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有 ______ (填仪器名称)。
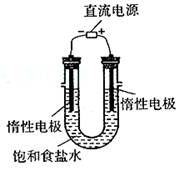
⑶电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2 (填“>”、“=”或“<”)2L,原因是 _____ 。装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为 ________ 。
⑷实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4====ZnSO4+H2↑
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
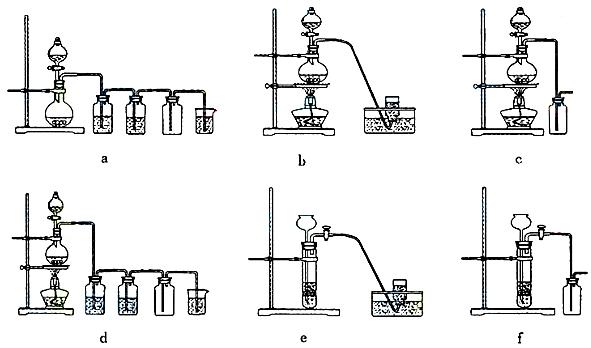
据此,从下列所给仪器装置中选择制备并收集H2的装置_____ (填代号)和制备并收集干燥、纯净Cl2的装置____ (填代号)。
可选用制备气体的装置:
(08年山东卷)13.NA代表阿伏加德罗常数,下列叙述错误的是()
A.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8%
B.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.一定温度下,1L0.5mol?L-1NH4Cl溶液与2L0.25mol?L-1NH4Cl溶液含NH4+物质的量不同
[2012·山东卷] 下列实验操作正确的是( )
A.中和滴定实验时,用待测液润洗锥形瓶
B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热
7.(08年山东卷)下列由事实得出的结论错误的是( )
A.维勒用无机物合成了尿素,突破了无机物与有机物的界限
B.门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新
C.C60是英国和美国化学家共同发现的,体现了国际科技合作的重要性
D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究为主的学科
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com