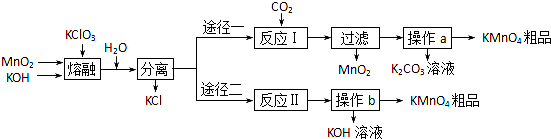
锂在原子能工业中具有十分独特的地位,被誉为“高能金属”,它推动着能源工业,尤其是电池技术的发展.盐湖卤水中锂的含量较高,资源丰富,提炼锂的价格低廉,成为国内外开发生产锂的主攻方向.把盐湖卤水自然日晒和冷冻,从卤水中析出食盐、泻利盐、钾盐镁矾和光卤石等一系列盐类,得到富含MgC1
2的浓缩母液,其中LiC1的浓度达10%以上.把浓缩母液经高温炉分解除去MgC1
2等一系列过程,最终得到金属锂.其主要生产工艺流程如下:
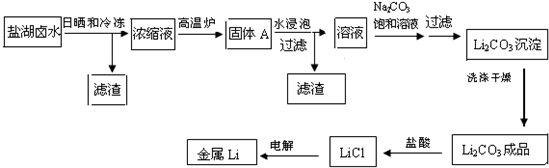
已知:Li
2CO
3在不同温度的溶解度如下表:
| 温度/℃ |
0 |
10 |
20 |
50 |
75 |
100 |
| Li2CO3的溶解度/g |
1.539 |
1.406 |
1.329 |
1.181 |
0.866 |
0.728 |
(1)写出浓缩母液在高温炉中分解的化学方程式
MgCl2+2H2O=Mg(OH)2+2HCl
MgCl2+2H2O=Mg(OH)2+2HCl
.
(2)写出盐酸与Li2CO3反应的离子方程式
Li2CO3+2H+=2Li++CO2↑+H2O
Li2CO3+2H+=2Li++CO2↑+H2O
.
(3)洗涤所得Li2CO3沉淀要用热水而非冷水,原因是
Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗
Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗
.
(4)熔融LiCl电解的环境是
de
de
a.氢气中 b.氮气中 c.空气中 d.真空中 e.He气.