
题目列表(包括答案和解析)
空气中SO2的来源主要是______的燃烧,以及______的冶炼和硫酸、磷肥、纸浆生产等产生的工业废气.
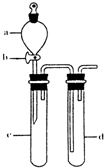 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.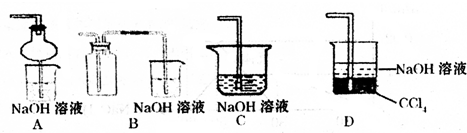
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
| SO2 | NO2 | PM10 | |||
| A | 98 | 23 | 67 | SO2 | Ⅱ |
| B | 47 | 29 | 35 | SO2 | Ⅰ |
| C | 62 | 40 | 113 | PM10 | Ⅲ |
| D | 42 | 76 | 59 | NO2 | Ⅰ |
煤是一种常用的燃料,由于煤燃烧产生的废气含有SO2、NO2和NO等多种有害气体和烟尘会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放
(1)将煤直接进行燃烧,造成环境污染的主要方面之一是形成硝酸型酸雨
①写出有关物质转化为硝酸的化学方程式
②以下是对硝酸型酸雨的若干项评价,其中正确的是
a:杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b:对电线,铁轨,桥梁,房屋等均会造成严重损害
c:导致臭氧层空洞
d:硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥。
(2)对煤用石灰石进行脱硫处理,过程中发生的方程式为:
(3)脱硫后,在废气中含有的不良气体是 ,它对环境的负面影响是 。
(4)检验脱硫后废气中是否含有SO2的简单方法是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com