
题目列表(包括答案和解析)
已知: (1)NH3(g)+HCl(g)=NH4Cl(s); △H1=-76kJ·mol-1
(2)NH3(g)+H2O(l)=NH3·H2O(aq); △H2=-35.1kJ·mol-1
(3)HCl(g)+HCl (aq); △H3=-72.3kJ·mol-1
(4)HCl (aq) NH3·H2O(aq) =NH4Cl(aq)+H2O(l); △H4=-52.3kJ·mol-1
(5)NH4Cl(s)=NH2Cl(aq); △H5=?
根据盖斯定律,则(5)方程式中的反应热△H5为
A.-335.7 kJ·mol-1 B.-16.3 kJ·mol-1
C.+16.3 kJ·mol-1 D.-83.7 kJ·mol-1
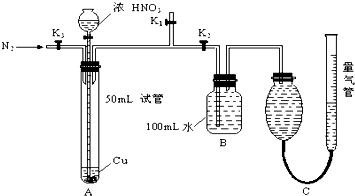
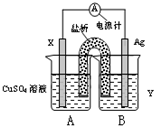 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.| 1 |
| 2 |
| 1 |
| 2 |
(2010 ·云南昆明)100克C不完全燃烧所得的产物中,CO占体积的![]() ,CO2占
,CO2占![]() ,且:[来源:Zxxk.Com]
,且:[来源:Zxxk.Com]
CO(g)+![]() O2(g) = CO2(g);DH =-282.57 kJ/mol
O2(g) = CO2(g);DH =-282.57 kJ/mol
C(s) + ![]() O2(g) = CO(g);DH =-110.3
O2(g) = CO(g);DH =-110.3![]() 5 kJ
5 kJ![]() /mol
/mol
与这些C完全燃烧相比,损失的热量为( )
A.-784.92 kJ kJ B.274.3 kJ C.784.92 kJ D.489.4 kJ
解析:由盖斯定律可得,碳不完全燃烧损失的热量为生成的CO完全燃烧放出的热量。所以损失的热量为![]()
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com