
题目列表(包括答案和解析)
(12分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
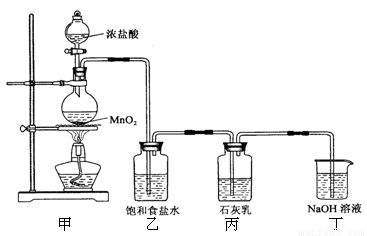
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是 ;乙装置的作用是______。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。

(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______。
(8分)、奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。实验操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A、凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B、定容时,俯视刻度线 C、定容时,仰视刻度线 D、移液时,有少量液体溅出
 (3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。其实凯氏定氮法的缺陷并不难弥补,只要先用三氯乙酸处理样品。三氯乙酸能让蛋白质形成沉淀,过滤后,分别测定沉淀和滤液中的氮含量,就可以知道蛋白质的真正含量和冒充蛋白质的氮含量。试求三聚氰胺中氮的含量为 。
(12分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。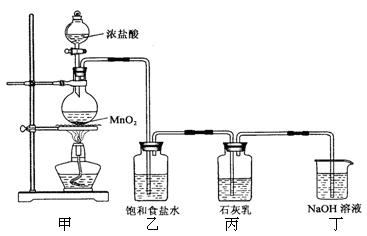
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是 ;乙装置的作用是______。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可 制得Ca(ClO)2______________g。
制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。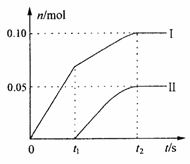
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______。
(12分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是 ;乙装置的作用是______。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______。
在 40mL0.5mol/L的氢氧化钠溶液中,通入一定量的硫化氢气体,充分反应后的溶液在低温条件下蒸干得白色固体8.48g.
(1)在标准状况下通入硫化氢气体的体积是________L,蒸干溶液所得白色固体的成分是________,其质量分别是________.
(2)如果所得固体成分中含有硫化钠和氢氧化钠,则通入的硫化氢气体的物质的量的n取值范围是________,蒸发溶液最后得白色固体的质量m的取值范围是________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com