氮元素及其化合物在国防科学技术生产中有重要应用.
(1)写出实验室制NH
3的化学反应方程式
.
(2)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,氢气的来源是水和碳氢化合物,写出以天然气为原料制取氢气的化学反应方程式
.
(3)在合成氨的原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H
2O(g)?CO
2(g)+H
2(g)△H<0,反应达到平衡后,为提高CO的转化率,可采取的措施有
,已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中,c(H
2O)﹕c(CO)不低于
,

(4)在容积为2L容器中发生反应CO(g)+H
2O(g)?CO
2(g)+H
2(g),已知c(CO)与反应时间t变化曲线Ⅰ,若在t
0时刻将容器的体积扩大至4L,请在图1中绘出c(CO)与反应时间t变化曲线Ⅱ.
(5)工业上尿素CO(NH
2)
2由CO
2和NH
3在一定条件下合成,其化学反应方程式为
.
(6)合成尿素,当氨碳比
=4,CO
2的转化率随时间的变化关系如图2所示.
①A点的逆反应速率v
逆(CO
2)
B点的正反应速率为v
正(CO
2)(填“>”、“<”或“=”).
②NH
3的平衡转化率为
.

 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示. 2Z
2Z 2Z
2Z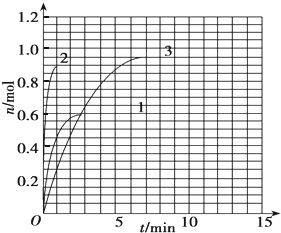
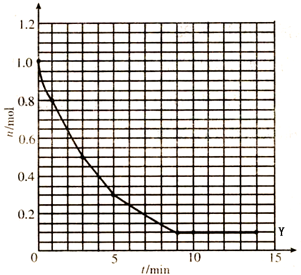 (2)体系中发生反应的化学方程式是
(2)体系中发生反应的化学方程式是
 在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.请回答下列问题:
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.请回答下列问题: