
题目列表(包括答案和解析)
乙醇的氧化反应
1、铜丝在酒精灯中灼烧
【实验装置】见图1
【实验步骤】
(1) 取一根铜丝,把其中一端绕成螺旋状。为什么?
(2) 点燃一盏酒精灯,把绕成螺旋状一端的铜丝移到酒精灯外
焰上灼烧,观察现象。
(3) 把螺旋状铜丝往酒精灯内焰移动,观察实验现象。
(4) 把螺旋状铜丝往酒精灯外焰移动,观察实验现象。
(5) 重复实验步骤3、4的操作。
【现象结论】
(1) 分步说明可观察到的实验现象
(2) 涉及到的化学反应式有 。
2、已知乙醇可以被强氧化剂重铬酸钾(K2Cr2O7,红棕色)的酸性溶液氧化成CH3COOH,还原产物为Cr3+(绿色),此实验原理可以用于检验汽车驾驶员是否酒后开车。请写出该反应的离子方程式 。
在氯化钴溶液中,四氯合钴(Ⅱ)离子与六水合钴(Ⅱ)离子间存在如下平衡:
![]()
又知:二氯化钴的水合物存在以下平衡,在加热时会逐步失水,并呈现不同的颜色:
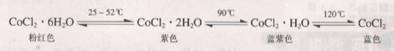
请你结合以上信息,完成下面的空格;
实验条件 | 实验内容 | 实验现象 | 结论与解释 |
浓度变化 | 在一支试管中加入约3mL0.5mol?L-1CoCl2 溶液;再慢慢滴加约6mL浓盐酸。 |
|
|
将上述试管中的溶液一分为二,置于两支试管中,向一支中加入约3mL蒸馏水,与第一支试管作对比。 |
|
| |
温度变化
| 取一支试管,加入3 mL95%乙醇溶液和少量(2-3小粒)氯化钴晶体,振荡使其溶解,再滴加蒸馏水,至溶液恰好呈粉红色,然后用酒精灯加热该试管片刻。 |
|
|
酯的水解 条件变化 | 取三只试管,编号为1、2、3,分别注入4 mL蒸馏水、4 mL5 mol?L-1 硫酸、4 mL10 mol?L-1的氢氧化钠溶液。 | 试管1:
试管2:
试管3: |
|
在1、2试管中各滴加2滴甲基橙指示剂,试管3中滴加2滴石蕊溶液,使三支试管中溶液的颜色分别为橙色、红色和蓝色。 | |||
在三支试管中各加入2 mL乙酸乙酯,振荡后用透明胶带纸对液相界面做好标记。将三只试管同时插入热水浴(65℃-70℃)中,加热6-10分钟。 |
| 实验方案 | 实现现象 | 结论 |
| 1取一定量的合金粉末,加过量的 |
粉末部分溶解,并有气体放出. | 合金中一定含有 |
| ②取步骤①所得滤渣,加过量的 |
滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有 |
(16分)为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案。请回答每个方案中提出的问题。
【方案I】
(1)称取碳酸钙样品 M g;
(2)加入过量盐酸;
(3)收集并测定生成的气体体积 V mL。
问题1:反应结束后,量气管中的显示如右图所示,接下来的操作是: ,读出甲管中液面的读数。
【方案II】
(1)称取碳酸钙样品 M g;
(2)用c mol/L 盐酸 V mL(过量)溶解样品;
(3)取溶解后的溶液![]() mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
问题2:列出本实验中所用到的主要仪器名称(除铁架台及附件、烧杯之外) 。
问题3:碳酸钙纯度计算公式 。
问题4:当碳酸钙溶解完全后,少量未溶的SiO2没过滤去,结果得到碳酸钙纯度________ (偏大、偏小或无影响)
【方案Ⅲ】
(1)称取碳酸钙样品 M g;
(2)加入足量c mol/L盐酸VmL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′ mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为M′g。
问题5:此方案中不需要的数据是 (填选项编号)。
A.c、V B.c′、V′ C. M′ D. M
问题6:为减少实验误差,步骤(3)、(5)过滤后都要对沉淀进行洗涤,如果步骤(3)未经洗涤,则测定的碳酸钙的纯度将 (偏大、偏小、无影响,下同);如果步骤(5)未经洗涤,则测定的碳酸钙纯度将 。
问题7:判断步骤(4)中Na2CO3溶液是否过量的方法是 。
(14分)某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们进行了下列探究:
【猜想】(1)甲同学认为可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液,而不能用澄清石灰水鉴别。
(2)乙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别。
依据是 。
(3)丙同学认为可用盐酸鉴别Na2CO3和NaHCO3固体。
【实验探究】
(1)甲同学:①将CaCl2溶液加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现盛有Na2CO3的试管产生了白色沉淀;②将澄清石灰水加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现两支试管中也都产生了白色沉淀。
此实验结果与猜想相同。
(2)乙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图1):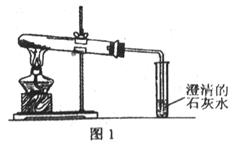
①加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO3时,乙同学观察到实验现象与①不同,证实了自己的猜想是合理的。
(3)丙同学在两支分别盛有少量Na2CO3、NaHCO3固体的试管中,各加入2 mL
2 mol/L的盐酸,观察到两支试管中均产生了大量气体,实验结果与猜想不一致,即得出不能用盐酸鉴别Na2CO3和NaHCO3。
【问题讨论】
(1)甲同学的两个实验中,大家对CaCl2与Na2CO3溶液的反应比较熟悉,该反应的离子方程式为 ;
(2)乙同学在加热Na2CO3固体时,开始产生少量气泡的原因是 ;在加热NaHCO3固体时,乙同学观察到的实验现象是 。
(3)丁同学认为丙同学的结论不对。丁同学认为对实验方案做一些改进,可用于鉴别碳酸钠与碳酸氢钠。他的改进方法是:称取各2.1 g两种固体,放入两个容积一样的气球中,在两只锥形瓶中各加入约25 mL 2 mol/L 的盐酸,分别将气球套在锥形瓶瓶口上,同时将气球中的固体同时倒入锥形瓶中,气球的膨胀比较 (填快或慢)的或最后气球比较 (填大或小)的是碳酸氢钠。
【拓展应用】
(1)要除去Na2CO3溶液中混有的少量NaHCO3,可加入适量的 溶液。
(2)要测定Na2CO3与NaHCO3固体混合物中Na2CO3的质量分数,可采用的方案有多种,请简述其中一种方案(写出简要步骤及要测定的数据,不要求写出如何用数据求出结果):
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com