
题目列表(包括答案和解析)
①过滤 ②NaOH ③BaCl2 ④盐酸 ⑤Na2CO3
当电解
(2)摩托罗拉公司研发了一种由甲醇(CH3OH)和氧气以及强碱作电解质溶液的新型手机电池。若放电过程中,甲醇完全氧化产生的CO2被碱充分吸收生成![]() 。则该电池反应的总离子方程式为________________________________________;甲醇在_____________极发生_____________反应。
。则该电池反应的总离子方程式为________________________________________;甲醇在_____________极发生_____________反应。
某蓄电池反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。
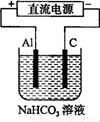
(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:

已知:
|
沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
开始沉淀时的pH |
2.3 |
7.5 |
5.6 |
6.2 |
|
完全沉淀时的pH |
3.9 |
9.7 |
6.4 |
8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
某蓄电池反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |


| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
Ⅰ.某同学做“铝热反应”的实验。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
|
物质 |
Al |
Al2O3 |
Fe |
Fe2O3 |
|
熔点/℃ |
660 |
2054 |
1535 |
1462 |
|
沸点/℃ |
2467 |
2980 |
2750 |
—— |
铝热反应方程式为 .
下列能与Al发生铝热反应的有 。(填序号)
A、MnO2 B、Na2O C、MgO D、FeO
据上表数据该同学推测,铝热反应所得到的熔融物应是铁铝合金。若证明上述所得的块状熔融物中含有金属铝,所用试剂是 ,该试剂溶质的电子式为 。
Ⅱ.某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的实验仪器有
_______________等。(填代号,下同)
A、试管;B、坩埚;C、烧杯;D、三角架;E、泥三角;F、洒精灯;G、铁架台;H、量筒
第2步:Iˉ溶液的获取。操作是将灰烬转移到烧杯中,加适量蒸馏水,用玻棒充分搅拌,煮沸,冷却,________。(填分离方法)
(3)第3步:氧化。取(2)中溶液少量依次加入合适的试剂。下列氧化剂最好选_________。
A、浓硫酸 B、新制氯水 C、KMnO4溶液 D、H2O2
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加_______溶液,证明海带中含碘。
氯碱工业中用离子交换膜法电解制碱的主要生产流程示意图如下:

依据上图完成下列填空:
(1)与电源正极相连的电极上所发生反应的电极反应式为____________________;与电源负极相连的电极附近,溶液的pH________(填“不变”、“升高”或“降低”)。
(2)工业食盐含Ca2+、Mg2+、Fe3+等杂质,精制过程中发生反应的离子方程式为_________________________________________________________________________。
(3)如果粗盐中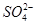 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去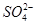 ,该钡试剂可以是________(填字母代号)。
,该钡试剂可以是________(填字母代号)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、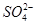 ,加入试剂的合理顺序为________(填字母代号)。
,加入试剂的合理顺序为________(填字母代号)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过______、冷却、______(填写操作名称)除去NaCl。
(6)由图示可知用离子交换膜法电解制碱工艺中________产品可循环使用。
(7)已知NaCl在60 ℃的溶解度为37.1 g,现电解60 ℃精制饱和食盐水1371 g,经分析,电解后溶液密度为1.37 g·cm-3,其中含有20 g NaCl,则电解后NaOH的物质的量浓度为________mol·L-1。
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意。)
题号
1
2
3
4
5
6
7
8
9
答案
B
B
A
D
C
C
A
D
B
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确的给2分,但只要选错一个,该小题就为0分。)
题号
10
11
12
13
14
15
16
17
18
答案
C
C
CD
BD
D
BC
B
BD
AC
三、(本题包括3小题,共34分)
19.(11分)
(1)CO32- + H2O
 HCO3- + OH- (2分)(配平、化学式错得0分,写等号扣1分)
HCO3- + OH- (2分)(配平、化学式错得0分,写等号扣1分)
(2)不再有气泡产生(或只有极少量气泡产生) (1分)
(3)若控制不准确温度过高Fe2+易被氧化;由于有氢气生成,明火加热不安全 (2分)
(两个方面各占1分)
(4)4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O (2分) (化学式错得0分,配平错扣1分)
(5)6.6 (2分) (多写单位g不扣分)
(6)循环使用 (2分)(具体说出如何循环使用同样得分,意思相近表达欠清晰扣1分)
20.(11分)
(1)2MnO4- + 5H
(化学式错得0分,配平错扣1分,漏↑扣1分,扣完为止)
(2)4 (2分)
(3)① 反应开始时:c(KMnO4)= =0.00067 mol?L-1 (1分)
=0.00067 mol?L-1 (1分)
反应时间: =
= =6.7min (1分)
=6.7min (1分)
KMnO4的平均反应速率:
ν(KMnO4)= =
= =1×10-4 mol?L-1?min-1 (1分)
=1×10-4 mol?L-1?min-1 (1分)
(一步完成计算且结果正确得3分,结果错误得0分。速率单位错误扣1分)
② 否(或:不可行) (1分) 取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应。(3分)
(基本思路错误得0分,思路正确未强调草酸过量扣1分,未强调体积相同扣1分)
21.(12分)
(1)7 (1分)
实验操作
预期现象和结论
步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管。
(1分)
白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl。(2分)
步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡。(1分)
固体溶解得无色溶液。(1分)
步骤3:向试管B中滴加过量的 Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置。(2分)
有白色沉淀生成,证明原白色粉末含有 K2SO4。(1分)
步骤4:取试管B中上层清液少量于试管C中,滴加 AgNO3溶液和1mol?L-1硝酸。(2分)
有白色沉淀生成,证明原白色粉末含有NaCl。(1分)
(3)
(NH4Cl的检验用NaOH溶液和红色石蕊试纸同样得3分;另取样品溶于水进行K2SO4的检验同样得2分;NaCl的检验必须包含有上述4个步骤的操作,共6分(着重号为关键点);步骤设计不合理,次序混乱酌情扣分。)
四、(本题包括3小题,共34分)
22.(10分)
(1)①  (1分)
(1分)
② 取形状大小相同的镁片和铝片分别与体积相同、浓度相同的稀盐酸反应,观察产生气泡的快慢 (2分)(操作1分,观察指标1分。着重号部分缺一处扣1分。用金属与沸水反应、等浓度盐溶液碱性比较等合理方法均得分,方案无可行性不给分。)
③ Na2SO3 + SO2 + H2O = 2NaHSO3 (2分)(化学式错得0分,配平错扣1分)
有白色胶状沉淀生成,有无色刺激性气味气体产生 (2分)
(各占1分,着重号部分有缺漏合扣1分)
(2)① H2PO4-、HCO3-、HPO42- (2分) ② 强 (1分)
23.(12分)
(1)Ba2+ + SO42- = BaSO4↓ Mg2+ + 2OH- = Mg(OH)2↓
Ca2+ + CO32- = CaCO3↓ Ba2+ + CO32- = BaCO3↓ (4分)
(每个1分。符号错误、漏↓得0分)
(2)2NaCl + 2H2O  2NaOH + H2↑+ Cl2↑ (2分)
2NaOH + H2↑+ Cl2↑ (2分)
(化学式错得0分,配平错扣1分,漏↑扣1分,漏条件扣1分,扣完为止)
(3)制漂白粉、生产盐酸、自来水消毒、制高纯硅、合成塑料等(任写2种) (2分)
(写对1个得1分。答案多于2个的按前2个答案评分。)
(4)蒸发浓缩(1分) 过滤(1分) (多写冷却不得分也不扣分)
蒸发过程中溶剂(水)大量减少,Na+浓度显著增加促进NaCl的沉淀溶解平衡向沉淀方向移动(或:Na+浓度显著增加抑止了NaCl的溶解) (2分)
(两个因素各占1分。后者从溶度积角度作答叙述正确也给分。)
24.(12分)
(1)增大 (1分)
(2)向左移 (1分)
 (3)(4分)
(3)(4分)
(各占2分,起点位置、曲线走势、终点与原曲线的相对高低等只要有一处错误则得0分。)
(4)(4分)
0.60(2分)
ν正_>_ν逆(2分)
(5)-787.0 (2分)(不带负号得0分,有效数字不准确扣1分。)
五、(本题包括1小题,共9分)
 25.(9分)
25.(9分)
(1) (2分)(有错即得0分)
 |
(2分)(漏系数n扣1分,漏条件不扣分)
 |
(2) (2分)

(3) (2分)
(漏系数2扣1分,不写条件不扣分)
(4)A、B (2分) (漏选1个扣1分,多选一个也扣1分,扣完为止。)
六、选做题(本题包括2小题,每小题10分。考生只能选做一题)
26.(10分)
 (1)① 碳碳双键、羧基 (2分)(写对一种得1分,错别字不给分,多写一个扣1分)
(1)① 碳碳双键、羧基 (2分)(写对一种得1分,错别字不给分,多写一个扣1分)
② (3分)
(2) (5分)

|