
题目列表(包括答案和解析)
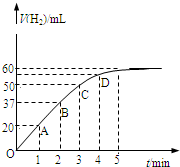 在恒温、恒容的密闭容器中发生如下反应:2HI(g)?H2(g)+I2(g),实验测定,在标准状况下产生氢气的体积和时间的关系如图所示.回答下列问题:
在恒温、恒容的密闭容器中发生如下反应:2HI(g)?H2(g)+I2(g),实验测定,在标准状况下产生氢气的体积和时间的关系如图所示.回答下列问题:在25℃,101Kpa下由HCHO(g)、H2和CO组成的混合气体共6.72g,其相对氢气的密度为14,将该气体与足量的氧气(标准状况)充分反应后的产物通过足量的Na202粉末,使Na202粉末增重的质量为 ( )
A.等于6.72g B.小于6.72g
C.大于6.72g D.无法计算
|
在25℃,101 Kpa下由HCHO(g)、H2和CO组成的混合气体共6.72 g,其相对氢气的密度为14,将该气体与足量的氧气(标准状况)充分反应后的产物通过足量的Na2O2粉末,使Na2O2粉末增重的质量为 | |
| [ ] | |
A. |
等于6.72 g |
B. |
小于6.72 g |
C. |
大于6.72 g |
D. |
无法计算 |
|
在25℃,101 Kpa下由HCHO(g)、H2和CO组成的混合气体共6.72 g,其相对氢气的密度为14将该气体与2.24 L氧气(标准状况)充分反应后的产物通过足量的Na202粉末,使Na202粉末增重的质量为 | |
A. |
等于6.72 g |
B. |
小于6.72 g |
C. |
大于6.72 g |
D. |
无法计算 |
|
在25℃,101 kPa下由HCHO(g)、H2和CO组成的混合气体共6.72 g,其相对氢气的密度为14,将该气体与2.24 L氧气(标准状况)充分反应后的产物通过足量的Na2O2粉末,使Na2O2粉末增重的质量为 | |
| [ ] | |
A. |
等于6.72 g |
B. |
小于6.72 g |
C. |
大于6.72 g |
D. |
无法计算 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com