
题目列表(包括答案和解析)
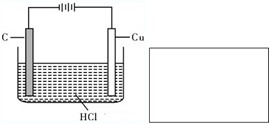 盐酸、硫酸和硝酸是中学常见的三种酸.
盐酸、硫酸和硝酸是中学常见的三种酸.
| ||
| ||

| ||
| H | + 4 |
| O | 2- 4 |
| O | - 3 |
| O | - 3 |

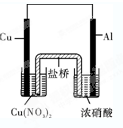
(1)写出A、B两试管中的实验现象:
A__________________________________、__________________________________(两种即可);B__________________________________。
(2)充分反应后,发现铜和硫酸都有剩余。在不补充浓硫酸的前提下,若使剩余铜片溶解,可再加入物质的化学式为____________________。
(3)测定剩余硫酸的物质的量时,先测铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量。他认为测定SO2的量的方法有多种,下列方案中不可行的是( )
A.将A产生的气体干燥后缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称量
B.将A产生的气体缓缓通入稀硫酸酸化的KMnO4溶液,加足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.将A产生的气体缓缓通入足量用HNO3酸化的Ba(NO3)2溶液,充分反应过滤、洗涤、干燥、称量沉淀
D.用排饱和NaHSO3溶液的方法测出干燥后装置A产生SO2气体的体积(已折算成标准状况)
(4)向反应后的溶液中加入足量的氧化铜,使剩余的硫酸转化为硫酸铜,过滤后将滤液加热浓缩,冷却制得硫酸铜晶体(CuSO4·xH2O),用加热法测定该晶体里结晶水x的值。其中一次实验的数据为:
坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
11.7 | G | 11.7 |
根据数据计算,判断x的实测值比理论值(x=5)_________(填“偏大”或“偏小”),实验中产生误差的原因可能是_________(填字母编号)。
A.硫酸铜晶体中含有不挥发杂质
B.加热失水后露置在空气中冷却
C.加热时有晶体飞溅出去
D.硫酸铜晶体(CuSO4·xH2O)在称量前晶体的表面吸收了水分
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com