
题目列表(包括答案和解析)
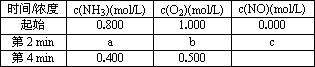
已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在容积固定的恒温密闭容器中充入NH3和O2发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g)在容积固定的恒温密闭容器中充入NH3和O2发生上述反应,容器内部分物质的物质的量浓度如下表:
(1)下列能说明该反应已经达到平衡状态的是________;
A.容器中气体平均摩尔质量不变
B.c(O2)不变
C.v(O2)=1.25v(NH3)
D.体系气体无颜色变化
E.体系压强不变
(2)在容器中加入正催化剂,则反应速率________(填“增大”“减小”“不变”;后同),降低容器的温度则反应速率________.
(3)反应在第2 min时,容器中压强与反应前之比为19∶18则a=________mol/L;0~2 min平均速率v(NH3)=________.第4 min时反应________(是、否)达到平衡.
(4)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因可能________.
(5)如果把该反应设计为原电池,NH3在原电池________极,电解质溶液中阴离子向________极移动.若果以NaCl为电解质,正极反应为:________.
已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) 在容积固定的恒温密闭容器中充入NH3和O2发生上述反应,容器内部分物质的物质的量浓度如下表:
4NO(g)+6H2O(g) 在容积固定的恒温密闭容器中充入NH3和O2发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | c(O2 )(mol/L) | c(NO)(mol/L) |
| 起始 | 0.800 | 1.000 | 0.000 |
| 第2 min | a | b | c |
| 第4 min | 0.400 | 0. 500 |
(1)下列能说明该反应已经达到平衡状态的是 ▲ (1分) ;
A.容器中气体平均摩尔质量不变 B.c(O2)不变 C.v(O2)= 1.25v(NH3) D.体系气体无颜色变化 E.体系压强不变
(2) 在容器中加入正催化剂,则反应速率 ▲ (填“增大”“减小”“不变”;后同),降低容器的温度则反应速率 ▲ (各1分)。
(3)反应在第2 min时,容器中压强与反应前之比为19︰18则a= ▲ mol/L;0~2 min平均速率v(NH3)= ▲ 。第4 min时反应 ▲ (是、否)达到平衡(各1分)
(4)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因可能 ▲ (1分)。
(5)如果把该反应设计为原电池,NH3在原电池 ▲ 极,电解质溶液中阴离子向 ▲ 极移动(各1分)。若果以NaCl为电解质,正极反应为:
▲ (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com