
题目列表(包括答案和解析)
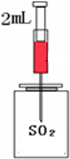
某化学课外活动小组的同学在学习NH3的性质时讨论:既然NH3具有还原性,能否像H2那样还原CuO呢?于是他们设计了如下实验装置(夹持装置未画出)进行实验。

请回答下列问题:
(1)仪器a的名称为______________;仪器b中可选择的试剂为______________;
(2)实验中观察到装置C中黑色CuO粉末变为红色固体,干燥管D增重,量气管内收集到无色无味的单质气体,上述现象可以证明NH3具有________性,写出相应的化学方程式_____________;
(3)E装置中浓硫酸的作用是________________________________
(4)读取气体体积前,应对装置F进行的操作是:________________________若读数时,量气管中的液面低于水准管的液面,则量气管中气体的体积将_____。(填“偏大”、“偏小”或“不变”)。
(5)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物,在酸性溶液中,Cu+易发生自身的氧化还原反应(2Cu+ →Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O: 。
(6)此套实验装置还可用于测定氨气的分子组成。若实验完毕,测得干燥管D增重m克,装置F测得气体的体积为n升(已折算成标准状况),则氨分子中氮、氢的原子个数比为________(用含m、n字母的代数式表示)
| ||
| ||
| ||
| ||
| H+ |
(Ⅰ)草酸晶体(H
(Ⅱ)无水草酸大约在
HOOC—COOH![]() CO2↑+CO↑+H2O↑
CO2↑+CO↑+H2O↑
(Ⅲ)H![]() BaC2O4↓+2H2O
BaC2O4↓+2H2O
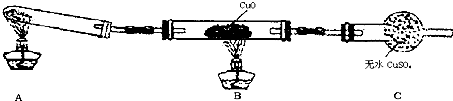
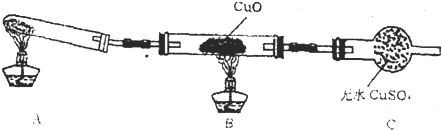
该小组采用下图所示的实验装置,通过实验验证无水草酸受热分解的产物,并利用反应产生的纯净CO气体来还原铁的某种氧化物(FezOy),以确定FexOy的组成。

请回答下列问题:
(1)实验所需的仪器如上图所示,各仪器的连接顺序为:e接________、_________接_________、_________接______。
(2)该组同学进行了下列实验操作,其操作先后顺序为________________。
①点燃B处左侧的酒精灯;
②检验实验装置的气密性;
③反应结束后,熄灭酒精灯;
④点燃C处的酒精灯,开始反应,并对装置B的d口处气体进行验纯,点燃尖嘴d处的酒精灯;
⑤向实验装置中装入药品
(3)D装置中澄清石灰水的作用________________________________,
B装置中澄清石灰水的作用________________________________________________。
(4)B装置中d处酒精灯的作用是________________________________。
(5)已知硬质玻璃管的质量为
(6)该小组设计的实验________________(填“有”或“无”)不妥之处。如有不妥,请说出不妥的原因________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com