根据图所示,按要求回答问题:
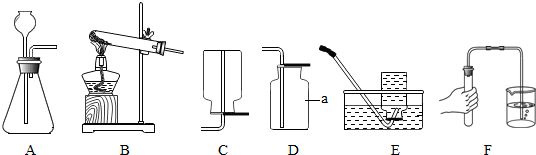
(1)图中仪器a的名称是
集气瓶
集气瓶
,图F实验的目的是
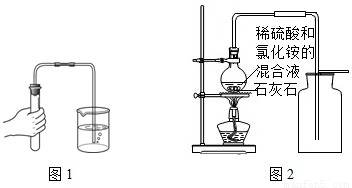
检查装置的气密性
检查装置的气密性
.
(2)实验室制取二氧化碳的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;所选用的发生装置是
A
A
(填序号).
(3)实验室加热氯酸钾和二氧化锰制氧气时,在该反应中质量和化学性质都没有改变的物质是
二氧化锰(或MnO2)
二氧化锰(或MnO2)
,收集氧气所选用的装置是
D或E
D或E
(填序号).
(4)在2011年5月喀左县初升高化学实验操作考试中,小红用A、E装置认真完成了双氧水和二氧化锰制取氧气的实验,请据此实验回答下列问题.
①双氧水和二氧化锰发生反应的化学方程式为
.
②在实验过程中,小军同学由于动作太慢,氧气还没有收集满,锥形瓶内的反应就已经停止.若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出可行的办法.方法是
通过长颈漏斗再加入适量的双氧水使反应继续进行或从长颈漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中(答案合理均可)
通过长颈漏斗再加入适量的双氧水使反应继续进行或从长颈漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中(答案合理均可)
.
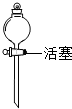
③小明同学认为,这套装置的缺点是不能控制反应随时发生、随时停止,造成了药品的浪费.为了解决小明提出的问题,请你对原实验装置加以改进,或设计新的简易实验装置,以便有效地控制双氧水的分解反应.
友情提示:你可从下列用品中选取,也可自行选用其它仪器.
 |
 |
 |
 |
 |
| 分液漏斗,通过旋转活塞能够逐滴滴加液体 |
装有二氧化锰的小布袋允许双氧水透过,不允许二氧化
锰透过 |
注射器 |
大试管 |
橡皮塞
(各种型号) |
请你在下表中至少写出两种方案:

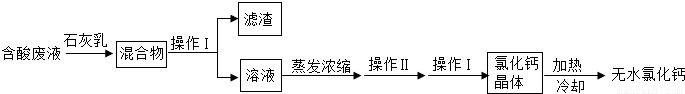
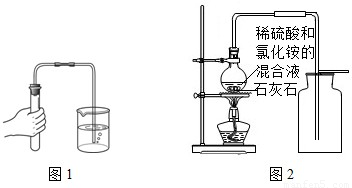
 实验室常用稀盐酸和石灰石反应制取二氧化碳.
实验室常用稀盐酸和石灰石反应制取二氧化碳.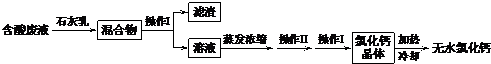
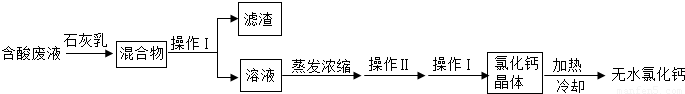








 x Fe + y H2O,Fe3C + 2H2
x Fe + y H2O,Fe3C + 2H2 3 Fe + CH4。
3 Fe + CH4。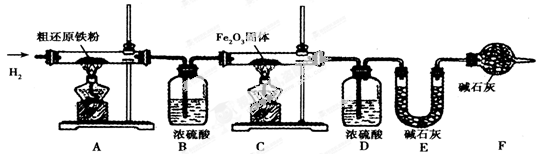
 3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3 CO2 + 6H2O + 8 Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。