碳及其化合物有广泛的用途.
(1)在电化学中,常用碳作电极:
①在酸性锌锰干电池中,碳棒作
极.
②若用碳棒和铁棒做电极电解饱和食盐水生产烧碱时,碳棒作
极,反应的离子方程式
.
(2)将水蒸气通过红热的碳可产生水煤气:C(s)+H
2O(g)?CO(g)+H
2(g)△H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H
2O的平衡转化率的措施是
.
A.升高温度 B.增加碳的用量
C.加入催化剂 D.用CO吸收剂除去CO
(3)将一定量的CO(g)和H
2O(g)通过某恒容的密闭容器中,发生反应:CO(g)+H
2O(g)?CO
2(g)+H
2(g)得到如下数据:
| 温度/℃ |
起始浓度mol/L |
平衡浓度mol/L |
| CO(g) |
H2O(g) |
H2(g) |
| 900 |
2.0 |
0.8 |
0.4 |
通过计算,该反应的平衡常数为:
.
(4)工业上把水煤气中的混合气体处理后,获得较纯的H
2用于合成氨:
N
2(g)+3H
2(g)?2NH
3(g)△H=-92.4kJ/mol某同学在不同实验条件下模拟化工生产进行实验,N
2浓度随时间变化如图1:
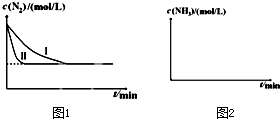
①与实验Ⅰ比较,实验Ⅱ改变的条件为:
.
②实验Ⅲ比实验I的温度要高,其它条件相同,请在图2画出实验Ⅰ和实验Ⅲ中NH
3浓度随时间变化的示意图.

 甲、乙两池电极材料如图所示.
甲、乙两池电极材料如图所示.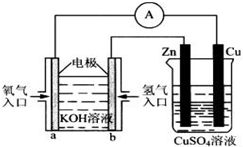 Ⅰ.用碳棒作电极,电解下列水溶液:①Na2SO4溶液 ②AgNO3溶液 ③KCl溶液 ④CuCl2溶液.通过相同电量时,阴极产生的气体物质的量相同的是(填序号)
Ⅰ.用碳棒作电极,电解下列水溶液:①Na2SO4溶液 ②AgNO3溶液 ③KCl溶液 ④CuCl2溶液.通过相同电量时,阴极产生的气体物质的量相同的是(填序号)
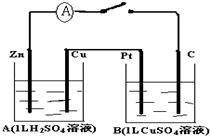 如图装置闭合电键时,电流计A的指针将发生偏转.试回答:
如图装置闭合电键时,电流计A的指针将发生偏转.试回答: