
题目列表(包括答案和解析)
石灰石的主要成分是碳酸钙(CaCO3),工业上常用煅烧石灰石的方法来制取生石灰(CaO),同时还会有大量的副产品——二氧化碳(CO2)被排放出来.为了净化和回收利用二氧化碳,北京化工二厂采用如图所示的石灰窑气体处理工艺:
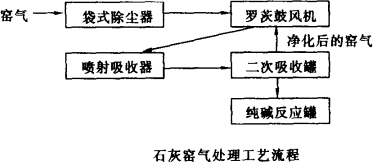
石灰窑气先经过两级除尘,经除尘净化的窑气由罗茨鼓风机吹到喷射吸收器中,在喷射吸收器中,窑气所含CO2用氢氧化钠(NaOH)溶液吸收生产纯碱(Na2CO3).净化后的窑气排入大气.请回答:
(1)工业制取CaO的化学方程式为________.
(2)NaOH吸收CO2的化学方程式为________.
(3)该工艺的意义有哪些?________
20世纪90年代我国的硫酸产量已达到1600万吨,这标志着我国硫酸工业取得飞速发展。工业生产硫酸的主要流程为:
① 煅烧黄铁矿4FeS2 + 11O2 点燃 2Fe2O3 + 8SO2; ② SO2 转化为 SO3;
SO3;
③ 用浓H2SO4吸收SO3  ; 请回答相关问题:
; 请回答相关问题:
1)工业上如何利用流程①中形成的Fe2O3炼铁(用化学方程式表示): 。
2)铁制品容易生锈是与空气中的 、 共同作用的结果,请你提出一条保护铁、防止铁生锈的方法 。
3)SO2是一种酸性氧化物,具有与CO2相似的化学性质。生产中会有部分SO2随尾气排入大气,造成环境污染。有人设计用氢氧化钙吸收尾气中的SO2,反应生成Ca SO3沉淀和水;请写出此反应的化学方程式
 2Fe2O3+8SO2;②SO2 转化为SO3;③用浓H2SO4吸收SO3;
2Fe2O3+8SO2;②SO2 转化为SO3;③用浓H2SO4吸收SO3;(8分)20世纪90年代我国的硫酸产量已达到1600万吨,这标志着我国硫酸工业取得飞速发展。工业生产硫酸的主要流程为:
①煅烧黄铁矿4FeS2 + 11O2 点燃 2Fe2O3+ 8SO2; ②SO2 转化为SO3;
③ 用浓H2SO4吸收SO3 ; 请回答相关问题:
(1)工业上如何利用流程①中形成的Fe2O3炼铁(用化学方程式表示): 。
(2)铁制品容易生锈是与空气中的 、 共同作用的结果,请你提出一条保护铁、防止铁生锈的方法 。
(3)SO2是一种酸性氧化物,具有与CO2相似的化学性质。生产中会有部分SO2随尾气排入大气,造成环境污染。有人设计用氢氧化钙吸收尾气中的SO2,反应生成Ca SO3和水;请写出此反应的化学方程式 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com