
题目列表(包括答案和解析)
科学家在不断深入的研究中,发现了一系列新的碳单质,对碳单质的研究现已发展成一门独立的学科——碳科学。1985年科学家发现的C60分子是由60个碳原子构成的,它的形状像足球(图C),因此又叫足球烯。1991年科学家又发现一种碳的单质——碳纳米管,它是由六边环形的碳原子构成的管状大分子(图D)。图A、B分别是金刚石和石墨的结构示意图。图中小黑点均代表碳原子。
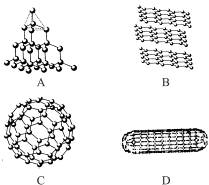
用你所学到的知识完成下列问题:
(1)碳纳米管由单层或多层石墨卷曲而成的,它是一种具有广阔发展前景的新型材料。关于碳纳米管的叙述不正确的是( )
A.不导电 B.充分燃烧生成二氧化碳
C.它和C60都是碳元素的同素异形体 D.它的性质和石墨的性质有相似之处
(2)金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是什么?
(3)常温下足球烯和碳纳米管的化学性质是否活泼?简要说明理由。
(4)请你设计一个方案,证明足球烯和碳纳米管都是由碳元素组成的。用文字简要叙述。
在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H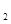 O外,还有H
O外,还有H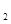 O
O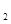 ;碳元素的氢化物除CH
;碳元素的氢化物除CH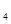 外,还有C
外,还有C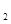 H
H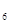 等;与之相似的氮元素的氢化物除外,还有N
等;与之相似的氮元素的氢化物除外,还有N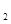 H
H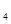 等。
等。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为 。
(2)该系列中的N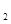 H
H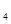 是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N
是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N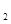 H
H 在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:
。
在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:
。
(3)该系列物中的NH 对农业、化学、国防工业具有重要意义。其合成原理为:
对农业、化学、国防工业具有重要意义。其合成原理为:
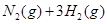


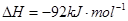
I.在一定温度下,将1.5molN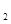 和6 molH
和6 molH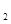 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
此时反应放出的热量为 kJ.
H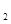 的转化率= 。
的转化率= 。
该温度下合成氨反应的平衡常数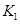 =
(只列数字表达式)
=
(只列数字表达式)
II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN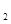 、bmolH
、bmolH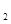 、cmolNH
、cmolNH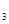 ,平衡时NH
,平衡时NH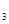 的物质的量分数为25%,则:
的物质的量分数为25%,则:
达到平衡时,I和II放出的热量 (填字母代号)
A。一定相等
B。前者一定小于后者
C。前者等于或小于后者
D。前者等于或大于后者
I和II合成氨的平衡常数分别为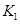 和
和 ,同
,同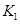
 (填“﹥”、“﹤”或
“=”)
(填“﹥”、“﹤”或
“=”)
欲使开始时反应正向进行,a的取值范围为 。
在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H![]() O外,还有H
O外,还有H![]() O
O![]() ;碳元素的氢化物除CH
;碳元素的氢化物除CH![]() 外,还有C
外,还有C![]() H
H![]() 等;与之相似的氮元素的氢化物除外,还有N
等;与之相似的氮元素的氢化物除外,还有N![]() H
H![]() 等。
等。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为 。
(2)该系列中的N![]() H
H![]() 是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N
是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N H
H![]() 在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式: 。
在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式: 。
(3)该系列物中的NH![]() 对农业、化学、国防工业具有重要意义。其合成原理为:
对农业、化学、国防工业具有重要意义。其合成原理为:
![]()
![]()
![]()
I.在一定温度下,将1.5molN 和6 molH
和6 molH![]() 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
此时反应放出的热量为 kJ.
H![]() 的转化率= 。
的转化率= 。
该温度下合成氨反应的平衡常数![]() = (只列数字表达式)
= (只列数字表达式)
II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN 、bmolH
、bmolH![]() 、cmolNH
、cmolNH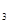 ,平衡时NH
,平衡时NH![]() 的物质的量分数为25%,则:
的物质的量分数为25%,则:
达到平衡时,I和II放出的热量 (填字母代号)
A。一定相等
B。前者一定小于后者
C。前者等于或小于后者
D。前者等于或大于后者
I和II合成氨的平衡常数分别为![]() 和
和![]() ,同
,同![]()
![]() (填“﹥”、“﹤”或“=”)
(填“﹥”、“﹤”或“=”)
欲使开始时反应正向进行,a的取值范围为 。
在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H O外,还有H
O外,还有H O
O ;碳元素的氢化物除CH
;碳元素的氢化物除CH 外,还有C
外,还有C H
H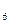 等;与之相似的氮元素的氢化物除外,还有N
等;与之相似的氮元素的氢化物除外,还有N H
H 等。
等。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为 。
(2)该系列中的N H
H 是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N
是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N H
H 在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式: 。
在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式: 。
(3)该系列物中的NH 对农业、化学、国防工业具有重要意义。其合成原理为:
对农业、化学、国防工业具有重要意义。其合成原理为: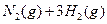


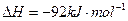
I.在一定温度下,将1.5molN 和6 molH
和6 molH 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则
此时反应放出的热量为 kJ.
H 的转化率= 。
的转化率= 。
该温度下合成氨反应的平衡常数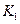 = (只列数字表达式)
= (只列数字表达式)
II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN 、bmolH
、bmolH 、cmolNH
、cmolNH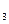 ,平衡时NH
,平衡时NH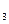 的物质的量分数为25%,则:
的物质的量分数为25%,则:
达到平衡时,I和II放出的热量 (填字母代号)
| A.一定相等 |
| B.前者一定小于后者 |
| C.前者等于或小于后者 |
| D.前者等于或大于后者 |
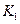 和
和 ,同
,同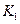
 (填“﹥”、“﹤
(填“﹥”、“﹤ ”或
”或 “=”)
“=”)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com