(2010?金华模拟)某研究性学习小组将一定浓度Na
2CO
3溶液滴入CuSO
4溶液中得到蓝色沉淀.
甲同学认为两者反应生成只有CuCO
3一种沉淀;
乙同学认为这两者相互促进水解反应,生成Cu(OH)
2一种沉淀;
丙同学认为生成CuCO
3和Cu(OH)
2两种沉淀.(查阅资料知:CuCO
3和Cu(OH)
2均不带结晶水)
Ⅰ.按照乙同学的理解Na
2CO
3溶液和CuSO
4溶液反应的化学反应方程式为
Na2CO3+CuSO4+H2O═Cu(OH)2↓+Na2SO4+CO2↑
Na2CO3+CuSO4+H2O═Cu(OH)2↓+Na2SO4+CO2↑
;在探究沉淀物成分前,须将沉淀从溶液中分离并净化.具体操作为①过滤②洗涤③干燥.
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分.
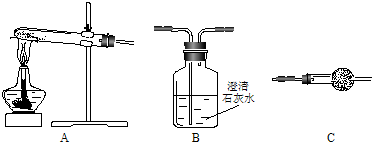
(1)各装置连接顺序为
A
A
→
C
C
→
B
B
.
(2)装置C中装有试剂的名称是
无水硫酸铜
无水硫酸铜
.
(3)能证明生成物中有CuCO
3的实验现象是
装置B中澄清石灰水变浑浊
装置B中澄清石灰水变浑浊
.
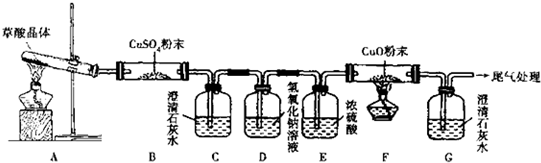
Ⅲ.若CuCO
3和Cu(OH)
2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成.
(1)装置C中碱石灰的作用是
吸收空气中的H2O 蒸汽和CO2
吸收空气中的H2O 蒸汽和CO2
,实验开始时和实验结束时都要通入过量的空气其作用分别是
开始时通入处理过的空气可以将装置中原有含H2O 蒸汽和CO2的空气排出;结束时通入处理过的空气可以将装置中滞留的H2O 蒸汽和CO2排出
开始时通入处理过的空气可以将装置中原有含H2O 蒸汽和CO2的空气排出;结束时通入处理过的空气可以将装置中滞留的H2O 蒸汽和CO2排出
.
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO
3的质量分数为:
.