(1)根据你掌握的知识判断,下列说法正确的是
ABF
ABF
.
A.用新制备的Cu(OH)
2悬浊液与病人尿液共热,可检验人尿液中是否含有葡萄糖
B.用量筒量取5.0ml.液体时俯视读数,会使液体体积小于5.0mL
C.用天平称量20.59某物质,砝码放在左盘,药品放在右盘
D.10%的硫酸和90%的硫酸等体积混合可配得50%的硫酸溶液
E.用灼烧闻气味的方法不能区别合成纤维和羊毛
F.紫外线、医用酒精能杀菌消毒,是因为使细菌的蛋白质性质改变
(2)将足量AgCl分别放入:①5ml水,②10ml 0.2mol?L
-1 MgCl
2溶液,③20ml 0.5mol?L
-1 NaCl溶液,④40ml 0.1mol?L
-1盐酸中溶解至溶液饱和,各溶液中Ag
+的浓度分别为a、b、c、d,它们由大到小的排列顺序是
a>d>b>c
a>d>b>c
.
(3)已知:
N
2(g)+3H
2((g)?2NH
3(g)△H
1=-92.4kJ/mol
2H
2(g)+O
2(g)=2H
2O(g)△H
2=-523.6kJ/mol
H
2O(g)=H
2O(l)△H
3=-44.0kJ/mol
根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N
2在催化剂(掺有少量Fe
2O
3的TiO
2)表面与水发生反应生成氨气,试写出此反应的热化学方程式:
2N2(g)+6H20(1)=4NH3(g)+302(g)△H=+1650kJ/mol
2N2(g)+6H20(1)=4NH3(g)+302(g)△H=+1650kJ/mol
.

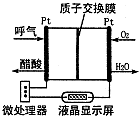
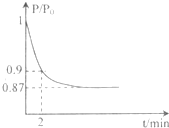 能源的开发利用与人类社会的可持续性发展息息相关.
能源的开发利用与人类社会的可持续性发展息息相关.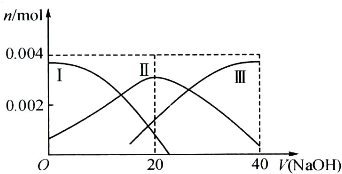
 氨气在化肥、致冷剂、有机合成工业中都有广泛应用.
氨气在化肥、致冷剂、有机合成工业中都有广泛应用.