钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,在自然界主要以钨(+6价)酸盐的形式存在.有开采价值的钨矿石之一黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO
4和MnWO
4,钨酸(H
2WO
4)酸性很弱,难溶于水.碳和金属钨在高温下会反应生成碳化钨.
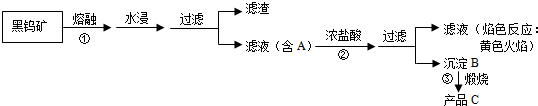
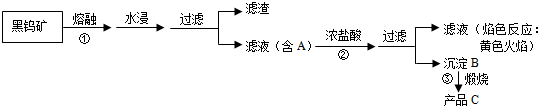
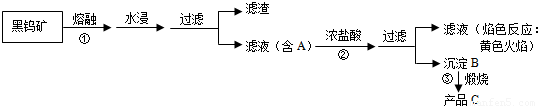
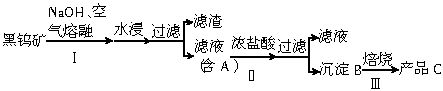
黑钨矿传统冶炼工艺的第一阶段是碱熔法:
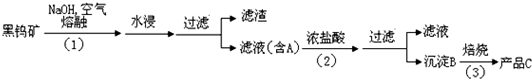
(1)黑钨矿浸入NaOH熔融液过程需通入大量空气,目的是为了使铁和锰转化为氧化物,其中一种红棕色的氧化物化学式为
;
(2)①已知A的主要成分为Na
2WO
4,请写出Na
2WO
4与浓盐酸反应的离子方程式
;
②上述流程中B、C都是钨的化合物,则步骤(3)中B→C转化属于
;(填四种基本反应类型之一)
(3)钨冶炼工艺的第二阶段则是用碳、氢气等还原剂把氧化钨(WO
3)还原为金属钨.对钨的纯度要求不高时,可用碳作还原剂.写出用碳还原氧化钨制取金属钨的化学方程式:
;为了获得可以拉制灯丝的高纯度金属钨,为什么不宜用碳而必须用氢气作还原剂?
.
(4)常温下,黑钨矿中FeWO
4和MnWO
4的溶度积常数分别为:K
sp(FeWO
4)=2.5×10
-12;K
sp(MnWO
4)=7.5×10
-16;欲将体积为1L含MnWO
4物质的量为0.6mol悬浊液全部转化为FeWO
4悬浊液,理论上可往MnWO
4悬浊液加入等体积一定浓度的FeCl
2溶液完成上述转化;请计算所加入FeCl
2溶液浓度为
mol/L(精确到小数点后一位),所以实际生产过程
(填“能”或“不能”)通过加入FeCl
2溶液的方法实现上述转化.(溶液混合体积变化可忽略)