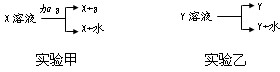Ⅰ.某学生设计了用新制氯水、KSCN溶液、0.1mol?L
-1FeCl
2溶液探究Fe
2+和Fe
3+的转化条件实验.操作为:取少量久置的FeCl
2溶液,滴加KSCN溶液,再滴入氯水.
(1)写出该实验发生的离子反应方程式
2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3
2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3
;
(2)实际操作中出现了异常现象,FeCl
2溶液滴入KSCN后就出现了浅红色,请分析最可能的原因
Fe2+被空气中的氧气氧化了
Fe2+被空气中的氧气氧化了
;
(3)由上述异常现象该同学联想到用KI淀粉溶液检验食用盐中IO
3-的实验,检验原理是:IO
3-+5I
-+6H
+=3I
2+3H
2O.为此进行了一系列探究实验如下:
| 实验 |
操作步骤 |
现象 |
| 1 |
取少量加碘食盐溶解,滴入几滴稀硫酸,滴入少量KI淀粉溶液,振荡 |
溶液变蓝 |
| 2 |
取少量NaCl溶解,滴入几滴稀硫酸,滴入少量KI淀粉溶液,振荡 |
溶液变蓝 |
| 3 |
取少量水… |
溶液变蓝 |
根据分析你认为实验3中的内容应为
滴入几滴稀硫酸,滴入少量KI淀粉溶液,振荡
滴入几滴稀硫酸,滴入少量KI淀粉溶液,振荡
,实验2、3异常现象最可能是发生了
4I-+O2+4H+=2I2+2H2O
4I-+O2+4H+=2I2+2H2O
离子反应,因此其实KI淀粉溶液并不能确定食盐中IO
3-的存在.
(4)经讨论,将KI换成其他试剂重新设计方案并取得了成功.你认为代替KI的可以是
ABC
ABC
A.Na
2SO
3 B.Vc C.FeSO
4 D.FeCl
3
Ⅱ.从X、Y两种溶液中分离固体X、Y的方法为
(1)实验甲中a应具有的性质为
易溶解X不溶于水不与X也不与水反应
易溶解X不溶于水不与X也不与水反应
;
(2)实验乙一般在
降温或蒸发
降温或蒸发
条件下实现,并借助下图中
A
A
装置分离出Y.