
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
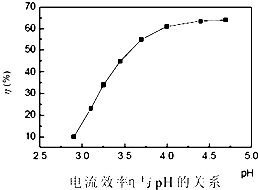 ČĖŌģ½šøÕŹÆĖįĻ“·ĻŅŗÖŠŗ¬ÓŠ“óĮæµÄNi2+”¢Mn2+”¢Co2+µČĄė×Ó£®Ä³³§¼¼ŹõČĖŌ±Éč¼ĘĮĖČēĻĀ·½°ø£¬Ź¹ÉĻŹöĄė×ÓµÄÅØ¶Č½µµĶµ½Åŷűź×¼£¬ĒŅµĆµ½ĮĖ“æ¶Č½ĻøßµÄÄų·Ū£®
ČĖŌģ½šøÕŹÆĖįĻ“·ĻŅŗÖŠŗ¬ÓŠ“óĮæµÄNi2+”¢Mn2+”¢Co2+µČĄė×Ó£®Ä³³§¼¼ŹõČĖŌ±Éč¼ĘĮĖČēĻĀ·½°ø£¬Ź¹ÉĻŹöĄė×ÓµÄÅØ¶Č½µµĶµ½Åŷűź×¼£¬ĒŅµĆµ½ĮĖ“æ¶Č½ĻøßµÄÄų·Ū£®| ½šŹōŌŖĖŲ | Ni | Mn | Co | Fe | Cu | Zn |
| ÅØ¶Č£Øg?L-1£© | 45 | 15 | 7.5 | ”Ü0.1 | ”Ü0.05 | ”Ü0.05 |
 ČĖŌģ½šøÕŹÆĖįĻ“·ĻŅŗÖŠŗ¬ÓŠ“óĮæµÄNi2+”¢Mn2+”¢Co2+µČĄė×Ó£®Ä³³§¼¼ŹõČĖŌ±Éč¼ĘĮĖČēĻĀ·½°ø£¬Ź¹ÉĻŹöĄė×ÓµÄÅØ¶Č½µµĶµ½Åŷűź×¼£¬ĒŅµĆµ½ĮĖ“æ¶Č½ĻøßµÄÄų·Ū£®
ČĖŌģ½šøÕŹÆĖįĻ“·ĻŅŗÖŠŗ¬ÓŠ“óĮæµÄNi2+”¢Mn2+”¢Co2+µČĄė×Ó£®Ä³³§¼¼ŹõČĖŌ±Éč¼ĘĮĖČēĻĀ·½°ø£¬Ź¹ÉĻŹöĄė×ÓµÄÅØ¶Č½µµĶµ½Åŷűź×¼£¬ĒŅµĆµ½ĮĖ“æ¶Č½ĻøßµÄÄų·Ū£®| ½šŹōŌŖĖŲ | Ni | Mn | Co | Fe | Cu | Zn |
| ÅØ¶Č£Øg?L-1£© | 45 | 15 | 7.5 | ”Ü0.1 | ”Ü0.05 | ”Ü0.05 |
¹¤ŅµÉś²śµÄ“æ¼īÖŠ³£ŗ¬ÓŠÉŁĮæNaClŌÓÖŹ”£ĪŖ²ā¶Øij“æ¼īѳʷµÄ“æ¶Č£¬»ÆѧæĪĶā»ī¶ÆŠ”×éÉč¼ĘĮĖČżÖÖŹµŃé·½°ø£ŗ
”¾·½°øŅ»”æȔѳʷČܽāŗó£¬¼ÓŹŌ¼ĮŹ¹CO32£³Įµķ£¬²ā¶Ø³ĮµķµÄÖŹĮ攣
”¾·½°ø¶ž”æÓĆ0.100 mol/LŃĪĖįµĪ¶Ø”£
”¾·½°øČż”æÓĆĻ”Ėį½«CO32£×Ŗ»ÆĪŖCO2£¬²ā¶ØCO2µÄÖŹĮ攣
½ā“š31-34Š”Ģā£ŗ
·½°øŅ»µÄ²Ł×÷²½ÖčÓŠ£ŗ¢Ł³ĘĮæ²¢Čܽāѳʷ£»¢Ś¼ÓČė×ćĮæµÄBaCl2ČÜŅŗ£»¢Ū¹żĀĖ£»¢ÜĻ“µÓ£»¢ŻøÉŌļ£»¢Ž³ĘĮæ²¢½ųŠŠŗćÖŲ²Ł×÷”£³ĘĮæŹ±ĖłŠč¶ØĮæŹµŃéŅĒĘ÷ĪŖ____________________”£ÅŠ¶ĻŹĒ·ń“ļµ½ŗćÖŲµÄ±ź×¼ŹĒ_____________________________________________________”£
·½°ø¶žµÄ¾ßĢå¹ż³ĢĪŖ£ŗ
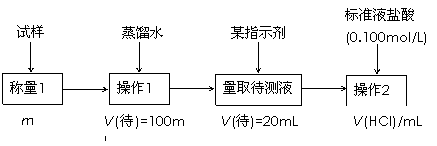 |
¢Ł²Ł×÷1ĖłŠčŅŖµÄŅĒĘ÷ÓŠ_____________________________________________”£
¢ŚµĪ¶ØŹ±Ń”ŌńµÄÖøŹ¾¼ĮĪŖ¼×»ł³Č”£µ±ČÜŅŗ____________________________________Ź±£¬ĖµĆ÷“ļµ½ĮĖµĪ¶ØÖÕµć”£
¢ŪĪŖ¼õÉŁÅ¼Č»Īó²ī£¬Ķس£µÄ“¦Ąķ°ģ·ØŹĒ_______________________________”£
¢ÜµĪ¶ØŹ±Čō׶ŠĪĘæÄŚÓŠÉŁĮæŅŗĢ彦³ö£¬Ōņ²ā¶Ø½į¹ū_________”££ØŃ”Ģī”°Ę«øß”±”¢”°Ę«µĶ”±”¢”°²»Ó°Ļģ”±£¬ĻĀĶ¬£©£¬ČōŹ¢×°Ī“ÖŖŅŗµÄ׶ŠĪĘæÓĆÕōĮóĖ®Ļ“¹ż£¬Ī“ÓĆĪ“ÖŖŅŗČóĻ“£¬²ā¶Ø½į¹ū_________”£
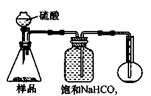
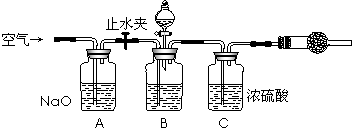 ·½°øČżµÄŹµŃé×°ÖĆČēĻĀĶ¼£ŗ
·½°øČżµÄŹµŃé×°ÖĆČēĻĀĶ¼£ŗ
²Ł×÷²½ÖčÓŠ£ŗ¢Ł¼ģ²é×°ÖƵÄĘųĆÜŠŌ£»¢ŚŌŚøÉŌļ¹ÜČװĀś¼īŹÆ»Ņ£¬³ĘĮæÖŹĮæĪŖW1 g£»¢Ū³ĘĮæW2 gѳʷװČė¹ćæŚĘæBÖŠ£»¢Ü¹Ų±ÕÖ¹Ė®¼Š£»¢Ż»ŗĀż¼ÓČėĻ”H2SO4ÖĮ²»ŌŁ²śÉśĘųĢåĪŖÖ¹£»¢Ž “ņæŖÖ¹Ė®¼Š£»¢ß»ŗ»ŗ¹ÄČėæÕĘųŹż·ÖÖÓ£¬ŌŁ³ĘĮæøÉŌļ¹Ü£¬ÖŹĮæĪŖW3 g”£
øĆ·½°øѳʷ֊“æ¼īµÄÖŹĮæ·ÖŹżĪŖ__________________________£ØÓĆ“śŹżŹ½±ķŹ¾£©”£
ÉĻĶ¼ÖŠ×°ÖĆAµÄ×÷ÓĆŹĒ_____________________”£×°ÖĆCµÄ×÷ÓĆŹĒ_____________________”£ÓŠĶ¬Ń§ČĻĪŖæÕĘųÖŠµÄĖ®ÕōĘų»į½ųČėøÉŌļ¹Üµ¼ÖĀ²āĮæ½į¹ū_____________(Ģī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°ĪŽÓ°Ļģ”±£©”£øĽų“ėŹ©æÉŅŌŹĒ______________________________________________”£
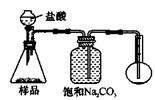
ČōÓĆĻĀĶ¼×°ÖƶŌѳʷ½ųŠŠ·ÖĪö£¬øł¾ŻĮæĘæÖŠŹÕ¼Æµ½µÄŅŗĢåµÄĢå»żĄ“¼ĘĖćѳʷ֊Ģ¼ĖįÄʵÄŗ¬Į攣ŌņĻĀĮŠ×°ÖĆÖŠ£¬×īŗĻĄķµÄŹĒ______”££ØŃ”ĢīŠņŗÅ£©
A B


C D
ѧŠ£ŹµŃéŹŅĻÖÓŠŗ¬ÉŁĮæNaClŌÓÖŹµÄNa2CO3¹ĢĢåѳʷ£¬Ä³»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§¾ö¶Ø²ā¶ØѳʷNa2CO3µÄÖŹĮæ·ÖŹż£¬¼×”¢ŅŅĮ½Ī»Ķ¬Ń§·Ö±šÉč¼Ę³öĻĀĮŠĮ½ÖÖŹµŃé·½°ø£ŗ

£Ø1£©¼×Ķ¬Ń§ÓĆĶ¼1ĖłŹ¾×°ÖĆ£¬Č”1.0gµÄ»ģŗĻĪļÓė×ćĮæĻ”ĮņĖį·“Ó¦ŗ󣬲ā¶Ø²śÉśµÄCO2ĘųĢåµÄĢå»ż”£ŹµŃéæŖŹ¼Ź±¼ģ²éøĆ×°ÖĆĘųĆÜŠŌµÄ·½·ØŹĒ”””” ”””””””””””””””””””””””””””” £»×¢ÉäĘ÷µÄČŻ»żÖĮÉŁŹĒ”””””” ””
A£®100mL”” B£®150mL”” C£® 200mL”” D£®250mL
Čē¹ū×¢ÉäĘ÷ÄŚµÄĘųĢåĢå»żŌö“ó168mL£Ø±ź×¼×“æö£©£¬ÄĒƓѳʷµÄ“æ¶ČŹĒ””””””””
£Ø2£©ŅŅĶ¬Ń§ÓĆĶ¼2×°ÖĆ²ā¶ØCO2µÄÖŹĮ棬øĆ×°ÖĆ“ęŌŚĆ÷ĻŌȱĻŻ£¬“Ó¶ųµ¼ÖĀŹµŃéĪó²ī£¬ĒėÄć·ÖĪöĘäÖŠŹ¹²ā¶Ø½į¹ūæÉÄÜĘ«“óµÄÖ÷ŅŖŌŅņ”””””””” £ØŠ“Ņ»Ģõ¼“æÉ£©£»Ź¹²ā¶Ø½į¹ūæÉÄÜĘ«Š”µÄÖ÷ŅŖŌŅņ”””””””””” £ØŠ“Ņ»Ģõ¼“æÉ£©”£
£Ø3£©±ūĶ¬Ń§ĄūÓĆ³Įµķ·ØÉč¼Ę³öĻĀĮŠŹµŃé·½°ø”£Ēė½«ŹµŃé²½Öč²¹³äĶźÕū”£²¢»Ų“šĻą¹ŲĪŹĢā£ŗ
¢Ł”””””””””””””” £¬¼ÓŹŹĮæÕōĮóĖ®Ź¹Ö®Č«²æČܽā£»
¢ŚĻņĖłµĆČÜŅŗÖŠ¼ÓČė¹żĮæµÄCaCl2ČÜŅŗŹ¹Ö®Éś³ÉCaCO3³Įµķ£»
¢Ū”””””””””””””””””””” £»¢Ü¼ĘĖćѳʷµÄÖŹĮæ·ÖŹż”£
”” ŌŚ²½Öč¢ŚÖŠČ·±£¼ÓČėµÄCaCl2ČÜŅŗ¹żĮæµÄ·½·ØŹĒ£ŗ””””””””””””””””””””””””””””
»ÆѧŹĒŌģø£ČĖĄąµÄæĘѧ£¬ŌŚČĖĢå±£½””¢Ņ½ĮĘĪĄÉśµČ·½Ćę×÷³öĮĖÖŲ“ó¹±Ļ×”£ĒėÄćÓĆĖłŃ§µÄ»ÆѧÖŖŹ¶½ā“šÓŠ¹ŲĪŹĢā”£
(1)Ź³Ę·°²Č«Óė½”æµĆÜĒŠĻą¹Ų”£ĻĀĮŠ×ö·Ø²»»įĪ£¼°ČĖĢå½”æµµÄŹĒ________”£
A£®ÓĆ”°ĖÕµ¤ŗģŅ»ŗÅ”±×÷Ź³Ę·Ģķ¼Ó¼Į
B£®ÕōĀųĶ·Ź±¼ÓČėŹŹĮæ“æ¼ī
C£®¼Ó¹żĮæŃĒĻõĖįÄĘŅŌ±£³ÖČāÖŹĻŹĆĄ
D£®°ŃĆ¹“óĆ×ĢŌ¾»ŗó¼ĢŠųŹ³ÓĆ
(2)µĶŃŖĢĒ»¼ÕßĆæĢģ¶¼Ó¦×¢ŅāÉćČėŅ»¶ØĮæŗ¬µķ·ŪµÄŹ³Īļ£¬ŅŌŹ¹ŃŖŅŗÖŠĪ¬³ÖŅ»¶ØÅØ¶ČµÄĘĻĢŃĢĒ”£ĒėÄćĮŠ¾ŁĮ½ÖÖø»ŗ¬µķ·ŪµÄŹ³Īļ£ŗ________”¢________”£
(3)ÓĶÕØŹ³Īļ²»ŅĖ¶ą³Ō£¬Ņņ³¤Ź±¼ä¼åÕØ»į²śÉśÓŠ¶¾ĪļÖŹ±ūĻ©Č©(C3H4O)£¬±ūĻ©Č©ŌŚæÕĘųÖŠĶźČ«Č¼ÉÕŹ±£¬Éś³É¶žŃõ»ÆĢ¼ŗĶĖ®”£ĒėŠ“³ö±ūĻ©Č©ĶźČ«Č¼ÉյĻÆѧ·½³ĢŹ½£ŗ
________________________________________________________________________ӣ
(4)Ź³ŃĪŹĒČĖĪ¬³ÖÕż³£ÉśĄķ»ī¶ÆµÄÖŲŅŖĪļÖŹ”£ČĖĢåĻø°ūÖŠŌ¼ŗ¬NaCl 0.9%£¬Ņ»°ć³ÉÄźČĖĆæČÕŠčNaClµÄĮæĪŖ4.5”«9 g”£
¢ŁÄ³²”ČĖŅņŹ³ŃĪÉćČėĮæ²»×ć£¬ŠčŅŖ²¹³äČÜÖŹÖŹĮæ·ÖŹżŌ¼ĪŖ0.9%µÄÉśĄķŃĪĖ®£¬ĻÖŅ½ÉśČ·¶ØĆæĢģĪŖĖū×¢Éä200 gÉśĄķŃĪĖ®£¬ŌņĆæĢģæÉĪŖĖū²¹³äŌ¼________gŹ³ŃĪ”£
¢ŚŠ”Ć÷Ķ¬Ń§øł¾ŻNaCl£«AgNO3===AgCl”ż(°×)£«NaNO3ÕāŅ»·“Ó¦ŌĄķ£¬¶ŌŅ»ĘæÉśĄķŃĪĖ®½ųŠŠ·ÖĪöŹ±£¬²»ÖŖµĄ¼ÓČėµÄĻõĖįŅųČÜŅŗÓėĀČ»ÆÄĘČÜŅŗŹĒ·ńĒ”ŗĆĶźČ«·“Ó¦£¬ÓŚŹĒĖūÉč¼ĘĮĖŅ»øöŹµŃé·½°ø½ųŠŠĢ½¾æ”£ĒėÄć°ļĖūĶźÉĘøĆŹµŃé·½°ø”£
|
Ģ½¾æ²½Öč |
æÉÄܹŪ²ģµ½µÄĻÖĻó |
½įĀŪ |
|
(1)Č”·“Ó¦ŗóµÄÉĻ²ćĒåŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó________ČÜŅŗ |
ČōÓŠ°×É«³ĮµķÉś³É |
________ČÜŅŗ¹żĮæ |
|
ČōĪŽ°×É«³ĮµķÉś³É |
»¹Šč½ųŠŠĻĀŅ»²½Ģ½¾æ |
|
|
(2)ĮķČ”·“Ó¦ŗóµÄÉĻ²ćĒåŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó________ČÜŅŗ |
|
|
|
|
|
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com