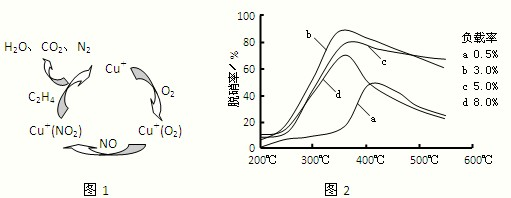
(2011?泰州一模)双氧水(过氧化氯)被称作“最清洁”的化学品,在纺织业和造纸业主要用作漂白剂,在化工合成中用作氧化剂和环氧化剂,在食品和医药工业中用作消毒剂、杀菌剂.目前,世界上过氧化氢的生产方法主要有电解法、葸醌法等.
I、电解法中成本最低的是过硫酸铵法
电解所用电槽以铂为阳极,以铅或石墨为阴极;NH
4HSO
4水溶液经阴极室,再作为阳极液从阳极室流出,得(NH
4)
2S
2O
8溶液,电解总反应式:2NH
4HSO
4(NH
4)
2S
2O
8+H
2↑;(NH
4)
2S
2O
8溶液送往水解器中减压水解、蒸发,蒸出过氧化氢的水溶液,剩余溶液流到阴极室再循环使用.
(1)写出过氧化氢的电子式
.
(2)写出水解器中(NH
4)
2S
2O
8溶液的水解方程式
(NH4)2S2O8+2H2O=2NH4HSO4+H2O2
(NH4)2S2O8+2H2O=2NH4HSO4+H2O2
.
(3)铂价格昂贵,试分析电槽阳极用铂不用铅的原因
铅会在阳极失电子生成阳离子进入溶液,且在阳极生成的S2O82-会氧化铅
铅会在阳极失电子生成阳离子进入溶液,且在阳极生成的S2O82-会氧化铅
.
(4)试分析水解器中使用减压水解、蒸发的原因
为了减少双氧水的分解损失
为了减少双氧水的分解损失
.
Ⅱ、葸醌法是国内外大规模生产过氧化氢普遍采用的方法,生产简易流程图如下所示:

其中,触媒为催化剂,工作液为乙基葸醌与有机溶剂的混合液,主要反应方程式为:

(1)写出流程图中加“?”的操作
萃取分液
萃取分液
.
(2)写出流程图中再生使用物质的名称
乙基葸醌
乙基葸醌
.
(3)根据双氧水生产的特点,工业液中有机溶剂的选择很重要.理想的有机溶剂应满足以下要求:①对乙基葸醌和氢乙基葸醌具有良好的溶解能力:②粘度低,沸点高,难挥发,着火点高;③低毒性.请分析再写出两点要求:④
机溶剂化学稳定性好,特别是抗氢化、抗氧化和抗水解能力好
机溶剂化学稳定性好,特别是抗氢化、抗氧化和抗水解能力好
;⑤
在水和双氧水中的溶解度小,和双氧水不反应,不至于产生爆炸危险,和水的密度差大,便于分离
在水和双氧水中的溶解度小,和双氧水不反应,不至于产生爆炸危险,和水的密度差大,便于分离
.





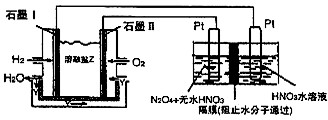 Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是
Ⅰ.X、Y、Z是短周期元素的三种常见氧化物.X跟水反应可生成一种具有还原性的不稳定的二元酸,该酸的化学式是