
题目列表(包括答案和解析)
| 电解 |
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
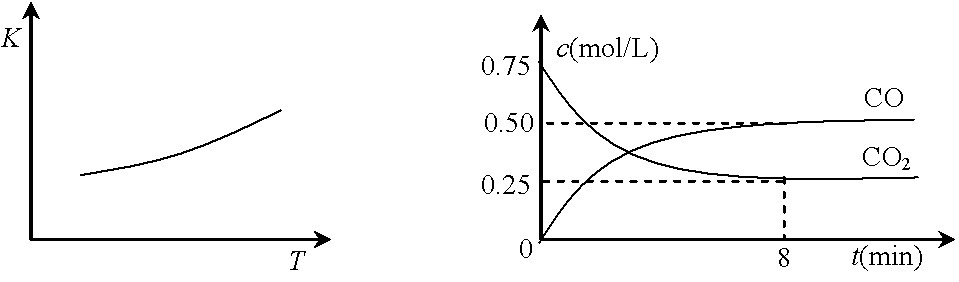
图甲 图乙
⑴该反应的平衡常数表达式K= ▲ 。
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。
8分钟内,CO的平均反应速率v(CO)= ▲ mol/(L·min)。
⑶下列措施中能使平衡时c(CO)/c(CO2)增大的是 ▲ (填序号)。
A.升高温度 B.增大压强
C.充入一定量CO D.再加入一些铁粉
⑷铁的重要化合物高铁酸钠是一种新型饮用水消毒剂,具有氧化能力强、安全性好等优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 ▲ 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化纳和水,该反应的离子方程式为 ▲ 。
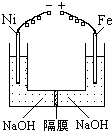 Ⅰ.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)
Ⅰ.一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g);△H>0
FeO(s)+CO(g);△H>0| c(CO) | c(CO2) |
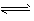 Mg2++2OH-①
Mg2++2OH-① 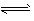 NH3·H2O+H+②
NH3·H2O+H+②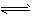 H2O③
H2O③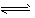 Mg2++2OH-①
Mg2++2OH-①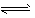 NH3·H2O②
NH3·H2O② M![]() s)
s)![]() Mg2++2OH- ①
Mg2++2OH- ①
NH![]() +
+ ![]()
![]()
![]() +H+
②
+H+
②
H++
OH-![]()
![]() ③
③
由于NH4+水解呈酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解。
乙同学的解释是:
![]() (s)
(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
NH![]() + OH-
+ OH-![]()
![]() ②
②
由于NH4Cl电离出的NH![]() 与
与![]() 电离出的OH-结合生成弱电解质
电离出的OH-结合生成弱电解质![]() ,对致反应①平衡右移,Mg(OH)2沉淀溶解。
,对致反应①平衡右移,Mg(OH)2沉淀溶解。
⑴丙同学能肯定哪位同学的解释合理,于是选取用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,你认为他选用的试剂是 (填编号)
A.NH4NO3 B.CH3COONH4
C.Na2CO3 D.NH3•H2O
⑵请你说明丙同学做出该选择的理由是 。
⑶丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解,由此推知,甲、乙哪位同学的解释更合理? (填甲或乙)。试写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com