
题目列表(包括答案和解析)

(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①碳酸钠,②碳酸氢钠,③碳酸氢铵,④氯化铵,⑤熟石灰,⑥氢氧化钠
若A中制取气体时只用了一种药品,则该药品是____________(填物质序号),并在图中空白处将实验装置图补充完整(使用下列简易装置图,固定装置省略;使用尺、规作图)

(2)该装置补充完整后,仍然存在一定缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①________________________________。
②________________________________。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用是________________。
②写出C中发生反应的化学方程式:________________________________;
③若A处试剂足量,则装置D中可以观察到的实验现象有____________。

试通过计算回答〔①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00〕:
(1)下列H2球较适合用于本实验的是_____________(填选项编号)。
A.500 mL H2球 B.896 mL H2球 C.1500 mL H2球
(2)反应至黑色全部变为红色止,测量H2球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g。则:
①参加反应的H2的质量为:______________;
②假设红色物质为单一物质,则红色物质的化学式为_______________________________。
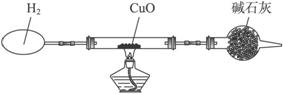
试通过计算回答〔①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00〕:
(1)下列氢气球较适合用于本实验的是_______________(填选项编号)。
A.500 mL 氢气球 B.896 mL 氢气球 C.1 500 mL 氢气球
(2)反应至黑色全部变为红色止,测得氢气球的体积变为220 mL,固体质量变为
①参加反应的H2的质量为_______________;
②假设红色物质为单一物质,则红色物质的化学式为_______________。
某课外活动小组设计了如下图所示的实验装置进行实验。回答下列问题:

⑴ 开始实验时弹簧夹e是打开的,A中发生反应的离子方程式为: ,B中可以观察到的现象是 。
⑵ 数分钟后夹上弹簧夹e,B中可以观察到的现象是 。
⑶ 如果开启活塞f放掉2/3液体,B中可观察到的现象是 ,
有关反应的化学方程式是
某课外活动小组设计了如下图所示的实验装置进行实验。回答下列问题:
⑴ 开始实验时弹簧夹e是打开的,A中发生反应的离子方程式为: ,B中可以观察到的现象是 。
⑵ 数分钟后夹上弹簧夹e,B中可以观察到的现象是 。
⑶ 如果开启活塞f放掉2/3液体,B中可观察到的现象是 ,
有关反应的化学方程式是
1.B 2.B 3.B 4.D 5.D 6.C 7.B 8.D 9.C 10.B
11.B 12.D 13.A 14.C 15.D 16.D 17.B 18.C 19.C 20.A
21.(8分)(1)取少量氨水,滴加酚酞试液,溶液呈红色,然后向其中加入少量CH3COONH4晶体,振荡,可看到红色变浅,说明氨水中存在电离平衡,说明氨水是弱碱。
(2)取少量NH4Cl晶体溶于水,滴加石蕊试液,溶液呈红色,说明NH4+水解,破坏了水的电离平衡,说明氨水是弱碱。(每小题4分)
22.(12分)(1)将等质量的氯酸钾分别加入两支试管中,向其中一支试管中加人少量一定质量的二氧化锰,用酒精灯分别加热,用排水法收集产生的气体。根据收集的氧气多少,可判断反应速率。
(2)用水溶解反应后的混合物,过滤并洗涤沉淀,干燥后称量,与最初加入量比较,可证明质量是否变化。
(3)将上述不溶物与浓盐酸混合加热,检验是否有氯气生成,可证明二氧化锰化学性质是否发生变化。
(4)将收集的气体用带火星的木条检验,可证明氯酸钾含氧元素。
(5)将(2)步骤作的滤液做焰色反应,可证明氯酸钾中是否含钾元素。
(6)将(2)步操作的滤液中加入用硝酸酸化的硝酸银溶液可证明氯酸钾中是否含氯元素。
(每步2分)
 25.(12分)(1)④③⑥ (2)G接F E接J(每空3分)
25.(12分)(1)④③⑥ (2)G接F E接J(每空3分)
(3)先向试管中加入一定量的稀H2SO4,(能没过锌片),将试管倾斜,小心地将锌片贴在试管壁上,塞好胶塞,连好装置,再将试管直立,使锌与稀H2SO4反应。(3分)
(4)设收集H2 VmL(标准状况),Zn的原子量为x
H2SO4+Zn=ZnSO4+H2↑
x 22.4L
W V×10-3L
x=  (3分)
(3分)
26.(8分)(1)C F G (2分)
(2)2Fe2+ +Cl2=2Fe3++2Cl- (2分)
(3)向漏斗里注入蒸馏水,使水面没过滤渣,等水自然流完后,重复操作2~3次。(2分)
(4)继续加热,放置干燥器中冷却,称量,至最后两次称得的质量差不超过 (2分)
(2分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com