
题目列表(包括答案和解析)
A.
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.(1)该反应的化学方程式为________,生成物NF3中氮原子的杂化方式为________,NF3分子空间构型为________;
(2)N、F两种元素的氢化物稳定性比较,NH3________HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式________;
(4)元素A基态原子的核外电子排布式为
1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如图,该离子化合物的化学式为________.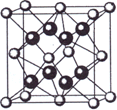
B.绿矾(FeSO4·7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体,反应原理为:
(NH4)2SO4+FeSO4+6H2O=(NH4)2SO4·FeSO4·6H2O↓.其流程可表示为: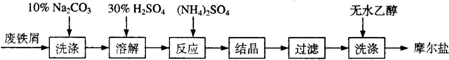
(1)洗涤中Na2CO3的主要作用是________.
(2)结晶过程中要加热蒸发溶剂,浓缩结晶.应加热到________时,停止加热.
(3)过滤是用下图所示装置进行的,这种过滤跟普通过滤相比,除了过滤速度快外,还有一个优点是________.
(4)用无水乙醇洗涤的目的是________.
(5)产品中Fe2+的定量分析:制得的摩尔盐样品中往往含有极少量的Fe3+.为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性条件下KMnO4标准液滴定的方法.称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸.用0.2 mol/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液10.00 mL.
①本实验的指示剂是________.(填字母)
A.酚酞
B.甲基橙
C.石蕊
D.不需要
②产品中Fe2+的质量分数为________.
|
将0.3 mol CaCl2溶于水配成4 L溶液,则2 L溶液里含有Cl-为 | |
A. |
9.03×1022个 |
B. |
1.806×1023个 |
C. |
0.6 mol |
D. |
0.4 mol |
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1)C元素在周期表中的位置 。
(2)A元素与水反应的离子方程式是 。
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式 。
(4)![]() 和
和![]() 均具有漂白性,二者的漂白原理 。(填“相同”或“不同”)
均具有漂白性,二者的漂白原理 。(填“相同”或“不同”)
(5)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
3H2+N2 ![]() 2NH3 △H=-92.4kJ·mol-1
2NH3 △H=-92.4kJ·mol-1
①当合成氨反应达到平衡后,改变某一外界条件 (不
改变![]() 、
、![]() 和
和![]() 的量),反应速率与时间的关
的量),反应速率与时间的关
系如右图所示。图中![]() 时引起平衡移动的条件可能
时引起平衡移动的条件可能
是 ,其中表示平衡混合物中![]() 的含量最
的含量最
高的一段时间是 。

②温度为T℃时,将2a mol![]() 和a mol
和a mol![]() 放入0.5 L 密闭容器中,充分反应后测得
放入0.5 L 密闭容器中,充分反应后测得![]() 的转化率为50%。则该反应的平衡常数为 。
的转化率为50%。则该反应的平衡常数为 。
将4 mol A 气体和2 mol B 气体在2 L 的容器中混合并在一定条件下发生如下反应, 2A(g) +B(g) 2C(g) 若经2 s 后测得C 的浓度为0.6 mol/L ;
现有下列几种说法:①用物质A 表示的反应的平均速率为0.3 mol/(L · s) ②用物质B 表示的反应的平均速率为0.6 mol/(L · s) ③ 2 s 时物质 A 的转化率为70 % ④2 s 时物质B 的浓度为0.7 mol/L 其中正确是( )。
A .①③ B .①④ C .②③ D .③④
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1)C元素在周期表中的位置 。
(2)A元素与水反应的离子方程式是 。
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式 。
(4)和
均具有漂白性,二者的漂白原理 。(填“相同”或“不同”)
(5)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
3H2+N2 2NH3 △H=-92.4kJ·mol-1
①当合成氨反应达到平衡后,改变某一外界条件 (不
改变、
和
的量),反应速率与时间的关
系如右图所示。图中时引起平衡移动的条件可能
是 ,其中表示平衡混合物中的含量最
高的一段时间是 。
②温度为T℃时,将2a mol和a mol
放入0.5 L 密闭容器中,充分反应后测得
的转化率为50%。则该反应的平衡常数为 。
第Ⅰ卷(选择题 共45分)
选择题 (1~15题,每题3分,共45分)
题 号
1
2
3
4
5
6
7
8
选 项
B
A
D
D
B
A
D
C
题 号
9
10
11
12
13
14
15
选 项
D
A
B
C
B
C
B
第Ⅱ卷(非选择题 共55分)
说明:1.合理答案均可酌情给分,但不得超过原题分数。
2.若化学方程式2分,不写条件扣1分,不配平扣1分。不写可逆符号扣1分,不得
负分。若化学方程1分,不写条件或不配平不得分。
3.除标注外,其余每空1分,不出现0.5分。
16.(共6分)
(1)4FeS2+11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
(2)C
(3)A B(2分。多选、错选均不得分;选对一个且正确得1分)
(4)氨水 (NH4)2SO3+H2SO4  (NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
(NH4)2SO4+H2O+SO2↑(写出NH4HSO3也可)
 17.(共7分)
17.(共7分)
(1)CH3CH2OH
CH2 CH2↑+ H2
O ①④⑤(多选、少选、错选均不
CH2↑+ H2
O ①④⑤(多选、少选、错选均不
得分)
 (2) 三角锥形 3Fe+8H++2NO
(2) 三角锥形 3Fe+8H++2NO
 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
(3)Al3+
+3AlO +6H2O
+6H2O  4Al(OH)
3↓ 2Al+2H2O+2OH
4Al(OH)
3↓ 2Al+2H2O+2OH
 2AlO
2AlO +3H2↑
+3H2↑
18.(共9分)
(1)2H2O2 2H2O+ O2↑
2H2O+ O2↑
(2)①③ (2分。多选、错选均不得分;选对一个且正确得1分)
(3)c(S2-)= [c(Na+)+c(H+)
[c(Na+)+c(H+) c (HS-)
c (HS-) c(OH
c(OH )]
)]
或c(S2-)= c (Na+)
c (Na+) c(HS
c(HS )
) c (H2S) (2分)
c (H2S) (2分)
(4)
19.(共8分)
(1)Fe3+、Al3+、Mg2+、H+(多写、少写、写错均不得分)
(2)SiO2+ Si+2CO↑
Si+2CO↑
AlO +CO2+ 2H2 O
+CO2+ 2H2 O  Al(OH)3↓+HCO
Al(OH)3↓+HCO (2分)
(2分)
(3)c d(2分。多选,错选均不得分;选对一个且正确得1分)
(4)电解 防止Mg2+水解,并带走水分,(答出“防止Mg2+水解”即可给分)
20.(共11分)
Ⅰ.(1)分液漏斗
B中棉花位置
①
②
③
④
所蘸试剂
现象
变红
褪色
体现的性质
还原性
(2)I2+SO2+2H2O
 4H+ +SO
4H+ +SO +2I
+2I
Ⅱ.(1)浓H2SO4
(2)Cl2+2I
 I2+2Cl
I2+2Cl b
b
(3)先由紫色变红色,后褪色
(4)5Cl2
+I2+6H2O  10Cl
10Cl +2IO
+2IO +12H+(2分)
+12H+(2分)
21.(共9分)
 |
22.(共5分)
(1)0.01 mol/L?s
(2)③④
(3)75%,<,
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com