
题目列表(包括答案和解析)
海洋是地球上最大的储水库,蕴含着丰富的化学资源。海水晒盐能够得到粗盐和卤水。
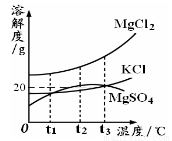
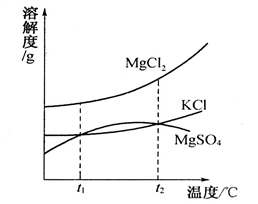
①卤水中含有MgCl2、KCl和MgSO4等物质,下图是三种物质的溶解度曲线。t2℃时,三种物质的饱和溶液中,溶质质量分数最小的是 。
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,
仍然为饱和溶液的是 。
③将饱和氯化镁溶液由t3℃冷却至t1℃,下列四种叙述中,
正确的是 (填序号)。
Ⅰ.溶液的质量不变 | Ⅱ.氯化镁的溶解度变小 |
Ⅲ.溶液中溶质质量不变 | Ⅳ.溶液中溶质质量分数变小 |
④在t3℃时,60克KCl的饱和溶液与60克MgCl2的饱和溶液中,溶质MgCl2与KCl的质量比为3∶1,则t3℃时MgCl2的溶解度为 。

海洋是地球上最大的储水库,浩瀚的海洋蕴藏着丰富的化学资源。
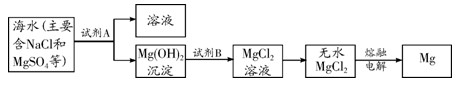
(1)目前世界上60%的镁是从海水中提取的。其主要步骤如下:

①提取Mg的过程中,试剂A可以选用_________,试剂B选用_________,由无水MgCl2制取Mg的反应类型为 。
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去 ;加入过量Na2CO3溶液的目的是 。
(2)从海水中制得的氯化钠除食用外,还常用作工业原料生产相应的化工产品,如工业上利用氯化钠和水在通电条件下生成烧碱、氢气和氯气,试写出上述化学方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com