
题目列表(包括答案和解析)
 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:| 金属 | 导电性 | 成本(¥/kg) | 密度 (g/cm3) |
强度 |
| 银 | 很好 | 2000 | 10.5 | 差 |
| 铝 | 较好 | 10 | 2.7 | 好 |
| 钢铁 | 一般 | 1.7 | 7.9 | 好 |
| A、巢湖的蓝藻现象与城乡生活污水、工农业废水等的排放有关 | B、大力发展低碳经济,提倡使用太阳能、风能的城市照明系统 | C、用加酶洗衣粉可以洗毛料衣服,水温越高效果越好 | D、用硫酸亚铁和氯气处理水,既能杀菌消毒又可去除水中的悬浮物 |
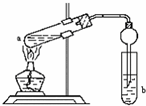 如图,在试管a中先加入2mL95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入2mL95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com