
题目列表(包括答案和解析)
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4?7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
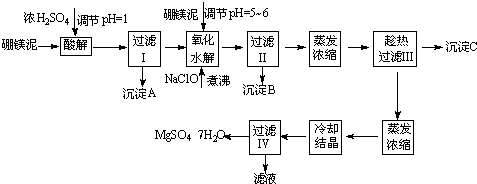
(04年广东卷)(8分)
维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知溶液的I2溶液进行滴定。该反应的化学方程式如下:

现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下。取10mL 6mol?L-1CH3COOH,加入100mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.2000g样品,溶解于上述冷却的溶液中,加入1mL淀粉指示剂,立即用浓度为0.05000mol?L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00mLI2溶液。
(1)为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
(2)计算样品中维生素C的质量分数。
(06年广东卷)纤维素是自然界最为丰富的可再生的天然高分子资源。
⑴纤维素可制备用于纺织、造纸等的粘胶纤维[成分是(C6H10O5)m],生产过程涉及多个化学反应。工艺简图如下:
 |
近来,化学家开发了一种使用NMMO加工纤维素的新方法,产品“LyoceⅡ纤维”成分也是(C6H10O5)m。工艺流程示意图如下:

①“LyoceⅡ纤维”工艺流程中,可充分循环利用的物质是 。
②与“LyoceⅡ纤维”工艺相比,粘胶纤维工艺中会产生含有 (只填非金属元素符号)的废物,并由此增加了生产成本。
③“LyoceⅡ纤维”被誉为“21世纪的绿色纤维”,原因是 。
⑵“LyoceⅡ纤维”工艺流程中的NMMO可按如下路线制备(反应条件均省略):
 |
其中,化合物I可三聚为最简单的芳香烃,化合物Ⅱ可使溴水褪色。
①化合物I也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物的化学式为 。
②化合物Ⅱ与氧气反应的原子利用率达100%,其化学方程式为 。
③关于化合物Ⅲ、Ⅳ的说法正确的是 (填代号)。
A.都可发生酯化反应 B.Ⅲ可被氧化,Ⅳ不可被氧化
C.都溶于水 D.Ⅲ可与钠反应,Ⅳ不可与钠反应
E.Ⅲ是乙醇的同系物 F.Ⅲ可由卤代烃的取代反应制备
④写出合成最后一步反应的化学方程式 。
(06年广东卷)纤维素是自然界最为丰富的可再生的天然高分子资源。
⑴纤维素可制备用于纺织、造纸等的粘胶纤维[成分是(C6H10O5)m],生产过程涉及多个化学反应。工艺简图如下:
 |
近来,化学家开发了一种使用NMMO加工纤维素的新方法,产品“LyoceⅡ纤维”成分也是(C6H10O5)m。工艺流程示意图如下:

①“LyoceⅡ纤维”工艺流程中,可充分循环利用的物质是 。
②与“LyoceⅡ纤维”工艺相比,粘胶纤维工艺中会产生含有 (只填非金属元素符号)的废物,并由此增加了生产成本。
③“LyoceⅡ纤维”被誉为“21世纪的绿色纤维”,原因是 。
⑵“LyoceⅡ纤维”工艺流程中的NMMO可按如下路线制备(反应条件均省略):
 |
其中,化合物I可三聚为最简单的芳香烃,化合物Ⅱ可使溴水褪色。
①化合物I也可聚合为在一定条件下具有导电性的高分子化合物,该高分子化合物的化学式为 。
②化合物Ⅱ与氧气反应的原子利用率达100%,其化学方程式为 。
③关于化合物Ⅲ、Ⅳ的说法正确的是 (填代号)。
A.都可发生酯化反应 B.Ⅲ可被氧化,Ⅳ不可被氧化
C.都溶于水 D.Ⅲ可与钠反应,Ⅳ不可与钠反应
E.Ⅲ是乙醇的同系物 F.Ⅲ可由卤代烃的取代反应制备
④写出合成最后一步反应的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com