
题目列表(包括答案和解析)
 实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 140℃ |
| 浓硫酸 |
| 140℃ |
| 高温 |
| 高温 |
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气。
(1)分别写出乙醇跟浓H2SO4反应生成①脱水生成CH2=CH2;②分子间脱水生成CH3CH2-O-CH2CH3;③SO2、CO2、水蒸气的化学方程式
① ;
② ;
③ ;
(2)二氧化硫是大气污染物之一,空
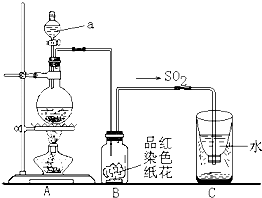
气中的二氧化硫随雨水下降形成酸雨。如下图实验装置,对酸雨的形成进行模拟并验证二氧化硫的部分性质,请回答:
①指出图中仪器a的名称: 。
②B装置中淡红色纸花的颜色逐渐变褪去,说明SO2有 性。
③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变 色。
④实验完毕后。为了使多余的二氧化硫被充分吸收,C装置应如何改进?
(用文字说明) 。
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气。
(1)分别写出乙醇跟浓H2SO4反应生成①脱水生成CH2=CH2;②分子间脱水生成CH3CH2-O-CH2CH3;③SO2、CO2、水蒸气的化学方程式
① ;
② ;
③ ;
(2)二氧化硫是大气污染物之一,空
气中的二氧化硫随雨水下降形成酸雨。如下图实验装置,对酸雨的形成进行模拟并验证二氧化硫的部分性质,请回答: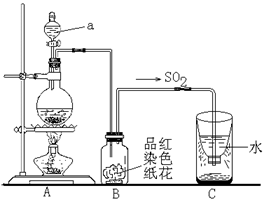
①指出图中仪器a的名称: 。
②B装置中淡红色纸花的颜色逐渐变褪去,说明SO2有 性。
③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变 色。
④实验完毕后。为了使多余的二氧化硫被充分吸收,C装置应如何改进?
(用文字说明) 。
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气。
(1)分别写出乙醇跟浓H2SO4反应生成①脱水生成CH2=CH2;②分子间脱水生成CH3CH2-O-CH2CH3;③SO2、CO2、水蒸气的化学方程式
① ;
② ;
③ ;
(2)二氧化硫是大气污染物之一,空
气中的二氧化硫随雨水下降形成酸雨。如下图实验装置,对酸雨的形成进行模拟并验证二氧化硫的部分性质,请回答:
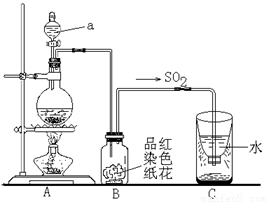
①指出图中仪器a的名称: 。
②B装置中淡红色纸花的颜色逐渐变褪去,说明SO2有 性。
③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变 色。
④实验完毕后。为了使多余的二氧化硫被充分吸收,C装置应如何改进?
(用文字说明) 。

题号
1
2
3
4
5
6
7
8
9
答案
A
D
B
D
C
B
C
B
D
题号
10
11
12
13
14
15
16
17
18
答案
B
D
B
A
A
C
D
B
A
19.(1)CH3CH2OH+4H2SO4  4SO2↑+CO2↑+7H2O+C;
2分
4SO2↑+CO2↑+7H2O+C;
2分
(2)④→③→①→②; 1分
(3)品红褪色; 混合气中有SO2。 溴水颜色变浅;
将SO2吸收完全。 混合气中已无SO2。 每空1分
(4)无水CuSO4 , 饱和石灰水, 每空1分
20.(1)过滤
(2)Al2O3; K2SO4和(NH4)2SO4 每空1分
(3)②Al3++3NH3?H2O=Al(OH) 3↓+3NH4+
③NaAlO2+HCl+H2O=Al(OH) 3↓+NaCl 每空2分
21.
A. CH3 CH3
| |
CH3-C-CH2-C-CH3
| |
CH3 CH3
B1. CH3 CH3
| |
CH3-C-C-CH2-CH3
| |
CH3 CH3
B2. CH2CH3
|
CH3CH2-C-CH2CH3
|
CH2CH3
B3. CH3 CH3 CH3
| | |
CH3-CH-C -CH-CH3
| 每空2分
CH3
22.②③④⑤⑥ ④⑥ 每空2分
23.(1)BnAm 1分 (2)An- 1分 An-+H2O=HA(n-1)-+OH- 2分
24.(1)H2 , O2 , O2 + H2O + 4e- = 4OH- H2 ? 2e- + 2OH- = 2H2O; 每空1分
(2)O2 + 2H2O + 4e- = 4OH- , CH4 + 10OH- + 8e- = CO32- + 7H2O 每空1分
CH4 + 2KOH+ 2O2 = K2CO3 + 3H2O。 2分
25.Ⅰ(1) CH3COOH +OH-=CH3COO-+H2O。
(2) 0.1 (3) 大于 , 小于,小于
(4) c (CH3COO- ) >c (Na+) > c (H+)> c (OH ? ) 每空1分
 Ⅱ(1)CO32-+H2OHCO3-+OH-
Ⅱ(1)CO32-+H2OHCO3-+OH-
向纯碱溶液中滴加数滴酚酞试液后,溶液显红色;然后逐滴加入氯化钙溶液直至过量,若溶液红色逐渐变浅直至消失,则说明上述观点。
(2)用pH试纸(或pH计)测常温下0.1mol?L-1纯碱溶液的pH,若pH<12,则该同学
的观点正确;若pH>12,则该同学的观点不正确。
(3)B、D 每空1分
26.(1)12.4g 3分 (2)49.18% 2分
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com