
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ08ФъЩНЖЋРэзлЁЄ29ЃЉББОЉАТдЫЛсЁАЯщдЦЁБЛ№ОцШМСЯЪЧБћЭщЃЈC3H8ЃЉЃЌбЧЬиРМДѓАТдЫЛсЛ№ОцШМСЯЪЧБћЯЉЃЈC3H6ЃЉЁЃ
ЃЈ1ЃЉБћЭщЭбЧтПЩЕУБћЯЉЁЃ
вбжЊЃКC3H8(g)=CH4(g)ЃЋHC![]() CH(g)ЃЋH2(g) ЁїH1=156.6 kJЁЄmolЃ1
CH(g)ЃЋH2(g) ЁїH1=156.6 kJЁЄmolЃ1
CH3CH![]() CH2(g)=CH4(g)ЃЋHC
CH2(g)=CH4(g)ЃЋHC![]() CH(g ) ЁїH2=32.4 kJЁЄmolЃ1
CH(g ) ЁїH2=32.4 kJЁЄmolЃ1
дђЯрЭЌЬѕМўЯТЃЌЗДгІC3H8(g)=CH3CH![]() CH2(g)ЃЋH2(g) ЕФЁїH= kJЁЄmolЃ1ЁЃ
CH2(g)ЃЋH2(g) ЕФЁїH= kJЁЄmolЃ1ЁЃ
ЃЈ2ЃЉвдБћЭщЮЊШМСЯжЦзїаТаЭШМСЯЕчГиЃЌЕчГиЕФе§МЋЭЈШыO2КЭCO2ЃЌИКМЋЭЈШыБћЭщЃЌЕчНтжЪЪЧШлШкЬМЫсбЮЁЃЕчГиЗДгІЗНГЬЪНЮЊ ЃЛЗХЕчЪБCO32ЃвЦЯђЕчГиЕФ ЃЈЬюЁАе§ЁБЛђЁАИКЁБЃЉМЋЁЃ
ЃЈ3ЃЉЬМЧтЛЏКЯЮяЭъШЋШМЩеЩњГЩCO2КЭH2OЁЃГЃЮТГЃбЙЯТЃЌПеЦјжаЕФCO2ШмгкЫЎЃЌДяЕНЦНКтЪБЃЌШмвКЕФpH=5.60ЃЌc(H2CO3)=1.5ЁС10-5 molЁЄL-1ЁЃШєКіТдЫЎЕФЕчРыМАH2CO3ЕФЕкЖўМЖЕчРыЃЌдђH2CO3![]() HCO3ЃЃЋHЃЋЕФЦНКтГЃЪ§K1= ЁЃЃЈвбжЊ10-5.60=2.5ЁС10-6ЃЉ
HCO3ЃЃЋHЃЋЕФЦНКтГЃЪ§K1= ЁЃЃЈвбжЊ10-5.60=2.5ЁС10-6ЃЉ
ЃЈ4ЃЉГЃЮТЯТЃЌ0.1 molЁЄL-1NaHCO3ШмвКЕФpHДѓгк8ЃЌдђШмвКжаc(H2CO3) c(CO32Ѓ)ЃЈЬюЁАЃОЁБЁЂЁА=ЁБЛђЁАЃМЁБЃЉЃЌдвђЪЧ ЃЈгУРызгЗНГЬЪНКЭБивЊЕФЮФзжЫЕУїЃЉЁЃ
ЃЈ08ФъЩНЖЋОэЃЉ13ЃЎNAДњБэАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаа№ЪіДэЮѓЕФЪЧЃЈЃЉ
AЃЎ10mLжЪСПЗжЪ§ЮЊ98%ЕФH2SO4ЃЌгУЫЎЯЁЪЭжС100mLЃЌH2SO4ЕФжЪСПЗжЪ§ЮЊ9.8%
BЃЎдкH2O2ЃЋCl2ЃН2HClЃЋO2ЗДгІжаЃЌУПЩњГЩ32gбѕЦјЃЌдђзЊвЦ2NAИіЕчзг
CЃЎБъзМзДПіЯТЃЌЗжзгЪ§ЮЊNAЕФCOЁЂC2H4ЛьКЯЦјЬхЬхЛ§дМЮЊ22.4LЃЌжЪСПЮЊ28g
DЃЎвЛЖЈЮТЖШЯТЃЌ1L0.5mol?L-1NH4ClШмвКгы2L0.25mol?L-1NH4ClШмвККЌNH4+ЮяжЪЕФСПВЛЭЌ
ЃЈ08ФъЩНЖЋОэЃЉЯТСаа№Ъіе§ШЗЕФЪЧЃЈЃЉ
AЃЎЦћгЭЁЂВёгЭКЭжВЮягЭЖМЪЧЬМЧтЛЏКЯЮя
BЃЎввДМПЩвдБЛбѕЛЏЮЊввЫсЃЌЖўепЖМФмЗЂЩњѕЅЛЏЗДгІ
CЃЎМзЭщЁЂввЯЉКЭБНдкЙЄвЕЩЯЖМПЩЭЈЙ§ЪЏгЭЗжСѓЕУЕН
DЃЎКЌ5ИіЬМдзгЕФгаЛњЮяЃЌУПИіЗжзгжазюЖрПЩаЮГЩ4ИіCЃCЕЅМќ
ЃЈ08ФъЩНЖЋОэЃЉБНБћЫсХЕСњЪЧвЛжжаЫЗмМСЃЌНсЙЙМђЪНЮЊЃК
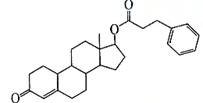
ЂХгЩБНБћЫсХЕСњЕФНсЙЙЭЦВтЃЌЫќФм_______ ЃЈЬюДњКХЃЉЁЃ
aЃЎЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋ bЃЎЪЙЫсадKMnO4ШмвКЭЪЩЋ
cЃЎгывјАБШмвКЗЂЩњвјОЕЗДгІ dЃЎгыNa2CO3ШмвКзїгУЩњГЩCO2
БНБћЫсХЕСњЕФвЛжжЭЌЗжвьЙЙЬхAЃЌдквЛЖЈЬѕМўЯТПЩЗЂЩњЯТСаЗДгІЃК
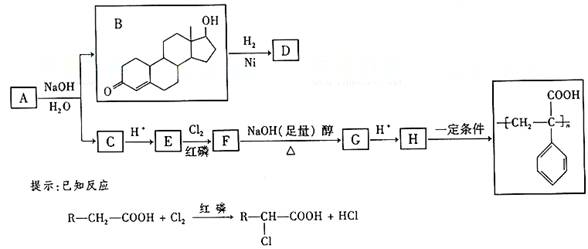
ОнвдЩЯаХЯЂЛиД№ЂЦЁЋЂШЬтЃК
ЂЦBЁњDЕФЗДгІРраЭЪЧ__________ ЁЃ
ЂЧCЕФНсЙЙМђЪНЮЊ__________ ЁЃ
ЂШFЁњGЕФЛЏбЇЗНГЬЪНЪЧ_________ ЁЃ
(8Зж)1918ФъЃЌLewisЬсГіЗДгІЫйТЪЕФХізВРэТлЃКЗДгІЮяЗжзгМфЕФЯрЛЅХізВЪЧЗДгІНјааЕФБивЊЬѕМўЃЌЕЋВЂВЛЪЧУПДЮХізВЖМФмв§Ц№ЗДгІЃЌжЛгаЩйЪ§ХізВВХФмЗЂЩњЛЏбЇЗДгІЁЃФмв§ЗЂЛЏбЇЗДгІЕФХізВГЦжЎЮЊгааЇХізВЁЃ

(1)ЭМIЪЧHIЗжНтЗДгІжаHIЗжзгжЎМфЕФМИжжХізВЪОвтЭМЃЌЦфжаЪєгкгааЇХізВЕФЪЧ
ЃЈбЁЬюЁАAЁБЁЂЁАBЁБЛђЁАCЁБЃЉЃЛ
(2)20ЪРМЭ30ФъДњЃЌEyringКЭPelzerдкХізВРэТлЕФЛљДЁЩЯЬсГіЛЏбЇЗДгІЕФЙ§ЖЩЬЌРэТлЃКЛЏбЇЗДгІВЂВЛЪЧЭЈЙ§МђЕЅЕФХізВОЭФмЭъГЩЕФЃЌЖјЪЧдкЗДгІЮяЕНЩњГЩЮяЕФЙ§ГЬжаОЙ§вЛИіИпФмСПЕФЙ§ЖЩЬЌЁЃЭМЂђЪЧNO2КЭCOЗДгІЩњГЩCO2КЭNOЙ§ГЬжаФмСПБфЛЏЪОвтЭМЃЌЧыаДГіNO2КЭCOЗДгІЕФШШЛЏбЇЗНГЬЪНЃК ЃЛ
(3)Й§ЖЩЬЌРэТлШЯЮЊЃЌДпЛЏМСИФБфЗДгІЫйТЪЕФдвђЪЧИФБфСЫЗДгІЕФЭООЖЃЌЖдДѓЖрЪ§ЗДгІЖјбджївЊЪЧЭЈЙ§ИФБфЙ§ЖЩЬЌЖјЕМжТгааЇХізВЫљашвЊЕФФмСПЗЂЩњБфЛЏЁЃЧыдкЭМЂђжазїГіNO2КЭCOЗДгІЪБЪЙгУДпЛЏМСЖјЪЙЗДгІЫйТЪМгПьЕФФмСПБфЛЏЪОвтЭМЃЛ
(4)НјвЛВНбаОПБэУїЃЌЛЏбЇЗДгІЕФФмСПБфЛЏ(ІЄH)гыЗДгІЮяКЭЩњГЩЮяЕФМќФмгаЙиЁЃМќФмПЩвдМђЕЅЕФРэНтЮЊЖЯПЊ1 mol ЛЏбЇМќЪБЫљашЮќЪеЕФФмСПЁЃЯТБэЪЧВПЗжЛЏбЇМќЕФМќФмЪ§ОнЃК
|
ЛЏбЇМќ |
CЃH |
ClЃCl |
CЁЊCl |
HЁЊCl |
|
МќФм/ kJЁЄmolЈC1 |
X |
243 |
330 |
432 |
вбжЊЃКЗДгІCH4(g)+Cl2(g)=CH3Cl(g)+HCl(g)ЃЛЁїH=-106kJ/molЃЌдђЩЯБэжаXЃН ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com