
题目列表(包括答案和解析)
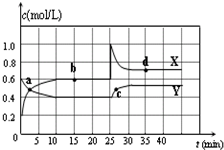
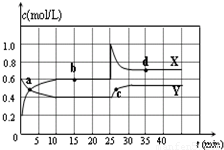
Ⅰ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。

(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
_________________________________________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________。
Ⅱ.下图是可逆反应X2+3Y2![]() 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是________
2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是________
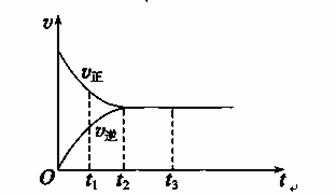
A.t1时,只有正方向反应
B.t2时,反应达到限度
C.t2~t3,反应不再发生
D.t2~t3,各物质的浓度不再发生变化
III.以下是关于化学反应2SO2 + O2 ![]() 2SO3 的两个素材:
2SO3 的两个素材:
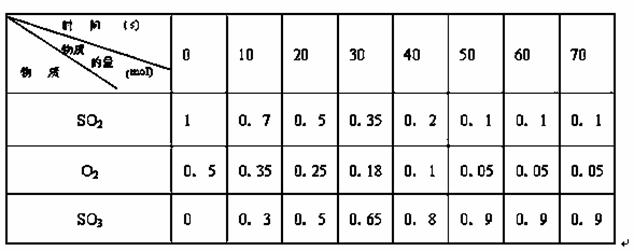
素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量
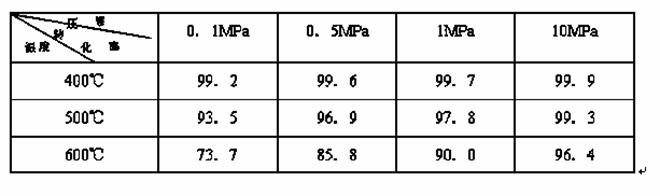
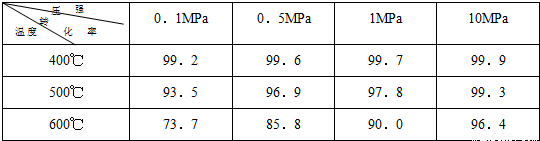
素材2:在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数)
从以上的两个素材中体会:
(1)根据素材1中计算20-30s期间,用二氧化硫表示的化学反应的平均速率为: 。
(2)根据素材2中分析得到,提高该化学反应限度的途径有: 。
(3)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件
是 。
 I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,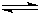 2X
2X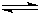 2X
2X 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是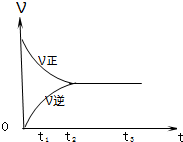
 2SO3 的两个素材:
2SO3 的两个素材: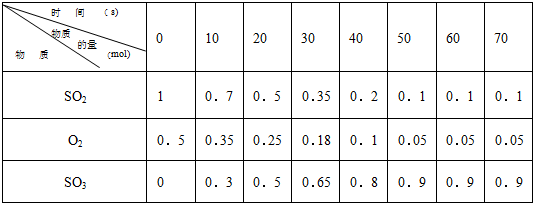
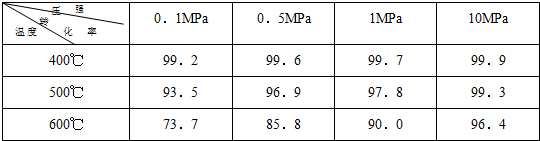
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示): 。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是 。
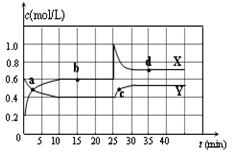
II.下图是可逆反应X2 + 3Y2 ![]() 2Z2 在反应过程中的反应速率(??)与时间(t)的关系曲线,
2Z2 在反应过程中的反应速率(??)与时间(t)的关系曲线,
下列叙述正确的是

A、t1时,只有正方向反应
B、t2时,反应到达限度
C、t2- t3,反应不再发生
D、t2- t3,各物质的浓度不再发生变化
III.以下是关于化学反应2SO2 + O2 ![]() 2SO3 的两个素材:
2SO3 的两个素材:
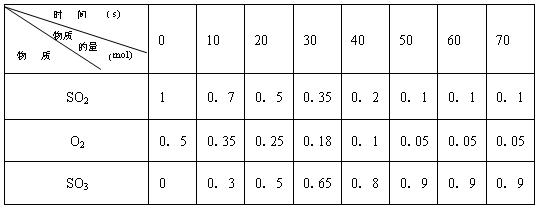
素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量
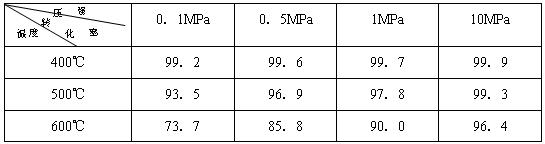
素材2:在不同条件下进行时SO2的转化率:(SO2的转化率是反应的SO2占起始SO2的百分数)
从以上的两个素材中体会:
(1)根据素材1中计算20-30s期间,用二氧化硫表示的化学反应的平均速率为: 。
(2)根据素材2中分析得到,提高该化学反应限度的途径有: 。
(3)根据素材1、素材2中分析得到,要实现素材1中SO2的转化率需控制的反应条件是 。
 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是______.
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是______.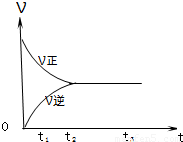
 2SO3 的两个素材:
2SO3 的两个素材: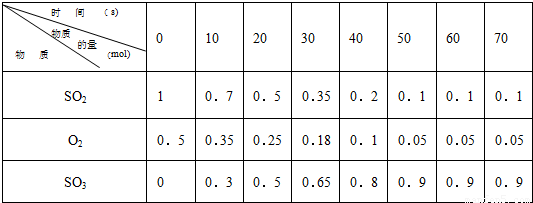
(14分)用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
Si3N4(s)+12HCl(g),在温度T0下的2 L密闭容器中,加入0.30 mol SiC14, 0.20 mol N2. 0.36 mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80 g
(1) SiCl4的平均反应速率为___
(2)平衡后,若改变温度,混合气体的平均相对分子质量与温度的关系如图所示,下列说法正确的是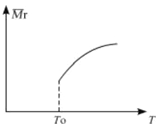
| A.该反应在任何温度下可自发进行 |
| B.若混合气体的总质量不变,表明上述反应己达到平衡状态 |
| C.其他条件不变,增大Si3N4的物质的量,平衡向左移动 |
| D.按3:2:6的物质的量比增加反应物,SiC14(g)的转化率降低 |

说明:
1. 本答案供阅卷评分使用,试题的参考解答是用来说明评分标准的,考生如按其他方法或步骤解答,正确的同样给分;有错的,根据错误的性质,参照评分标准中相应的规定评分。
2. 化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3. 化学方程式、离子方程式未配平的,都不给分。
4. 计算只有最后答案而无演算过程的,不给分。
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. A 2. D 3. B 4. A 5. C 6. D 7. C 8. C 9. D 10. D 11. B 12. C 13. B 14. D 15. A 16. D 17. A 18. C 19. A 20. B 21. B 22. D 23. B 24. C 25. A
第Ⅱ卷(非选择题,共50分)
二、(本题包括4小题,共22分)
26.(共4分)3,28,9,1,14(2分) 0.1(2分)
27.(共6分,每空2分)(1)0.01 mol/(L?s) (2)> 乙
 28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
O2+2H2O+4e-===4OH-
29.(共9分,每空1分)(1)AlCl3 Al2O3 Fe
(2)铝热 焊接钢轨,冶炼钒、铬、锰等金属(答出一种即可)
(3)3Fe+4H2O高温====Fe3O4+4H2
(4)① 2Al+2OH-+2H2O===2AlO-2+3H2↑ ② Al3++3AlO-2+6H2O===4Al(OH)3↓
(5)氨水
三、(本题包括2小题,共15分)
30.(共7分)(1)I-、Fe2+、Al3+(3分) HCO-3、NO-3(2分)
(2)4Fe(OH)2+O2+2H2O===4Fe(OH)3(1分)
(3)AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3(1分)
31.(共8分,每空1分)(1)Mg2++2OH-===Mg(OH)2↓(1分)
(2)碱式滴定管、酸式滴定管(1分) (3)酚酞(1分) 酚酞的变色范围最接近中性,滴定终点时,pH为8.2~10,Mg(OH)2不会溶解,不影响测定结果(1分)
(4)偏低(2分) (5)7.5 %(2分)
四、(本题包括2小题,共13分)
32.(共4分)解:n(Cu)==0.09 mol,n(HNO3)=2.0 mol/L×
==
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O ………………………………(1分)
3 8
=
因为< 所以硝酸过量 ……………………………………(1分)
n(NO)=×n(Cu)=×0.09 mol=0.06 mol ……………………………………(1分)
溶液中n(NO-3)=0.3 mol-0.06 mol=0.24 mol
c(NO-3)==1.6 mol/L ……………………………………………………(1分)
答:溶液中NO-3 的物质的量浓度为1.6 mol/L。
(此题的评分原则是:判断过量2分,算出NO-3 的浓度2分)
 33.(共9分)解:合金溶解于盐酸时所发生的反应有:
33.(共9分)解:合金溶解于盐酸时所发生的反应有:
Mg+2HCl===MgCl2+H2↑,2Al+6HCl===2AlCl3+3H2↑ ………………(1分)
根据图示,加NaOH溶液至130 mL过程中,发生的反应为:
NaOH+HCl===NaCl+H2O MgCl2+2NaOH===Mg(OH)2↓+2NaCl
AlCl3+3NaOH===Al(OH)3↓+3NaCl ………………………………………(1分)
当NaOH溶液由130 mL加至150 mL时,发生的反应为:
Al(OH)3+NaOH===NaAlO2+2H2O …………………………………………(1分)
(1)n(Mg)=n[Mg(OH)2]==0.15 mol ………………………………(1分)
m(Mg)=0.15 mol×
n(Al)=n[Al(OH)3]==0.1 mol ……………………………………(1分)
m(Al)=0.1 mol×
(2)据题意,在加入NaOH溶液130 mL时,溶液中n(Na+)=n(Cl-) …………(1分)
Na+ 全部来自NaOH,Cl- 全部来自盐酸,故n(HCl)=130×10
c(HCl)==6.5 mol/L …………………………………………………(1分)
答:原合金中Al、Mg的质量分别是
(此题的评分原则是:化学方程式或离子方程式共3分,算出铝的质量2分,算出镁的质量2分,算出盐酸的浓度2分。如未写化学方程式或离子方程式,计算结果正确者,镁、铝的质量各3分,盐酸的浓度3分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com