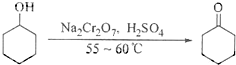(2009?江苏)环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:
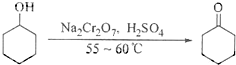
环己醇、环己酮和水的部分物理性质见下表:
| 物质 |
沸点(℃) |
密度(g-cm-3,200C) |
溶解性 |
| 环己醇 |
161.1(97.8)* |
0.9624 |
能溶于水 |
| 环己酮 |
155.6(95)* |
0.9478 |
微溶于水 |
| 水 |
100.0 |
0.9982 |
|
括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na
2Cr
2O
7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多.实验中将酸性Na
2Cr
2O
7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应.反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物.
①酸性Na
2Cr
2O
7溶液的加料方式为
缓慢滴加
缓慢滴加
.
②蒸馏不能分离环己酮和水的原因是
环已酮和水形成具有固定组成的混合物一起蒸出
环已酮和水形成具有固定组成的混合物一起蒸出
.
(2)环己酮的提纯需要经过以下一系列的操作:a蒸馏,收集151-156℃的馏分;b 过滤;c 在收集到的馏分中加NaCl固体至饱和,静置,分液;d 加入无水MgSO
4固体,除去有机物中少量水.
①上述操作的正确顺序是
cdba
cdba
(填字母).
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需
漏斗、分液漏斗
漏斗、分液漏斗
.
③在上述操作c中,加入NaCl固体的作用是
增加水层的密度,有利于分层
增加水层的密度,有利于分层
.
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有
3
3
种不同化学环境的氢原子.